|
|||||||||||||||
Все документы, представленные в каталоге, не являются их официальным изданием и предназначены исключительно для ознакомительных целей. Электронные копии этих документов могут распространяться без всяких ограничений. Вы можете размещать информацию с этого сайта на любом другом сайте.
МИНИСТЕРСТВО ПРОМЫШЛЕННОСТИ, НАУКИ И ТЕХНОЛОГИЙ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Правила организации чистых
производств
и контроля качества изделий
медицинского назначения из полимеров,
тканых и нетканых материалов,
имеющих контакт с кровью
ПР 64-05-001-2002
2002
Предисловие
1 РАЗРАБОТАНЫ Государственным унитарным предприятием Государственным научно-исследовательским институтом медицинских полимеров.
Исполнители: докт. техн. наук, академик МАРЭ Г.А. Матюшин; канд. техн. наук А.С. Беличенко; канд. техн. наук Б.П. Пашинин; Н.Б. Васильковкая; канд. хим. наук Г.И. Донцова; Е.С. Яворская; Н.М. Иванова
2 ПРИНЯТЫ И ВВЕДЕНЫ В ДЕЙСТВИЕ Распоряжением Министерства промышленности, науки и технологий Российской Федерации от 15 апреля 2003 г. № Р-19
3 ВВЕДЕНЫ ВПЕРВЫЕ
СОДЕРЖАНИЕ
Правила организации чистых производств и контроля качества изделий медицинского назначения из полимеров, тканых и нетканых материалов, имеющих контакт с кровью
Дата введения 2003-04-15
1. Общие положения
Настоящий документ устанавливает правила организации и контроля чистых производств полимерных изделий, тканых и нетканых материалов медицинского назначения, контактирующих с кровью. Правила распространяются на производства, изготавливающие следующие изделия медицинской техники:
- инфузионные, эксфузионные и трансфузионные устройства однократного применения;
- контейнеры для заготовки, разделения, хранения и транспортирования крови и ее компонентов однократного применения;
- контейнеры для розлива инфузионных растворов и кровезаменителей однократного применения;
- различные магистрали и трубки из полимерных материалов к аппаратам искусственного кровообращения;
- внутривенные катетеры однократного применения;
- шприцы инъекционные однократного применения в комплекте с иглами инъекционными однократного применения;
- фильтры вязаные и тканые для фильтрации крови и кровезаменителей;
- искусственные вязаные сосуды для имплантации;
- мембраны для тонкой очистки и стерилизации препаратов крови.
Документ разработан на основе «Правил GMP», «Good manufacturing practice», руководящего материала GMP по производству стерильных изделий медицинской промышленности (EUCOMED), «Правил производства лекарственных средств европейского сообщества (GMP ЕС)», ОСТа 42-510-98 «Правила организации производства и контроля качества лекарственных средств (GMP)».
Правила разработаны по результатам обследования отечественных производств изделий медицинского назначения из полимерных материалов, тканых и нетканых материалов медицинского назначения, контактирующих с кровью.
Документ предусматривает современный комплексный подход к решению проблемы обеспечения качества медицинской продукции, направленный на удовлетворение требований и потребностей потребителя.
Документ учитывает применение систем контроля для гарантирования качества продукции и связанные с этим стандарты системы гарантирования качества.
Контроль качества продукции проводится в соответствии с технологическим регламентом производства продукции и нормативно-технической документацией (ТУ, ОСТ и ГОСТ) на нее.
Настоящий документ следует использовать в качестве базовой структуры примера, на котором предприятие-изготовитель может основывать конкретное производство продукции требуемого качества. Использование его должно обеспечить производство медицинских изделий на современном уровне и гарантировать высокое качество продукции.
При проектировании, строительстве и реконструкции указанных производств должны соблюдаться санитарные и строительные нормы и правила, а также требования настоящих «Правил». Действующие производства, транспортирование и эксплуатация медицинских изделий должны соответствовать санитарным и гигиеническим правилам и санитарно-эпидемиологическим нормам.
Все действующие на предприятиях отрасли правила и инструкции по технике безопасности и промышленной санитарии должны быть приведены в соответствие с настоящими правилами.
При разработке отраслевых технологических регламентов, технических условий на оборудование, сырье, полуфабрикаты, продукцию и других документов и нормативов должны учитываться требования настоящих правил.
Особенностью технологического процесса производства изделий медицинского назначения из полимерных материалов являются повышенные требования к чистоте воздушной среды производственных помещений и к выпускаемой продукции. Для производственных помещений в зависимости от применения и выполняемых в них операций установлены определенные классы чистоты (таблица 2).
При сдаче в эксплуатацию вновь строящихся цехов и после реконструкции цехов и участков чистые производственные помещения должны быть аттестованы по ГОСТу Р ИСО 14644-4-2002 «Чистые помещения и связанные с ними контролируемые среды. Проектирование, строительство и ввод в эксплуатацию».
Практика оптимального изготовления стерильных медицинских изделий представляет сумму усилий, требуемых для обеспечения необходимого количества продукции, соответствующей ее конечному назначению.
Основные принципы ее следующие:
- система отбора поставщиков сырья и комплектующих;
- единая система производства и обеспечения качества;
- раздельная ответственность за изготовление и обеспечение качества;
- необходимые условия, оборудование и материалы;
- обученный персонал;
- профессионально подготовленная документация для изготовления и обеспечения качества;
- документальная информация о выпущенных партиях продукции;
- обеспечение адекватного хранения и транспортирования продукции;
- система валидации процессов и квалификации: проектной документации, монтажа, функционирования и эксплуатации оборудования чистых помещений и др.
- система обнаружения и выбраковывания негодной продукции;
- система учета претензий потребителей и отзыва поставленной продукции.
2. Терминология (определения)
В настоящем документе используются следующие определения:
|
Термин |
Определение |
|
Асептическое производство |
Асептическое изготовление медицинских изделий в контролируемой окружающей среде, в которой обеспечение материалами, воздухом, оборудованием и персоналом регулируется так, чтобы загрязнение микроорганизмами и механическими частицами не выходило за установленные пределы. |
|
Зона асептического производства (ЗАП) |
Участок асептического производства с контролируемой окружающей средой, в которой обеспечение воздухом, материалами, оборудованием и персоналом регулируется так, чтобы загрязнение микроорганизмами и механическими частицами не выходило за установленные пределы. |
|
Стерилизация |
Процесс, обеспечивающий удаление или инактивацию соответствующими методами до уровня отсутствия жизнеспособных микроорганизмов в изделии. |
|
Критический процесс (зона, операция, параметр и т.д.) |
Процесс (зона, операция, параметр и т.д.), который может быть причиной изменения качества промежуточной или готовой продукции. |
|
Критическая поверхность |
Поверхность в критической производственной зоне, находящаяся в непосредственной близости к асептическим операциям и представляющая риск для продукции. |
|
Партия |
Определенное количество сырья, промежуточного продукта и готовой продукции. Количество в одной партии может быть определено, например, временем изготовления, временем (интервалом времени) стерилизации, количеством продукции, изготовленной из одной партии сырья и (или) сопровождаемым одним документом о качестве продукции. |
|
Чистое помещение (Clean room) |
Помещение (комната) специально спроектированное, построенное и используемое помещение, укомплектованное необходимыми инженерными системами и оборудованием, в котором счетная концентрация аэрозольных частиц и концентрация жизнеспособных микроорганизмов (КОЕ) в воздушной среде поддерживаются в пределах не выше заданного, соответствующего определенному классу «чистоты», и в котором по мере необходимости, контролируются другие параметры (например, температура, относительная влажность, перепад давления). |
|
«Чистое» помещение в оснащенном состоянии |
Состояние «чистого» помещения, в котором все инженерные системы и технологическое оборудование находятся в работающем состоянии. |
|
«Чистое» помещение в функционирующем состоянии |
Состояние «чистого» помещения, в котором все инженерные системы и технологическое оборудование функционируют в режимах, соответствующих требованиям регламента, в присутствии необходимого количества работающего персонала. |
|
Карантин |
Состояние материалов или продуктов, ожидающих разрешения на дальнейшее использование, выдаваемое контролером качества. |
|
Карантинная зона |
Изолированная зона, используемая для хранения всех материалов и продуктов, подлежащих карантину. |
|
Микрофлора окружающей среды |
Среда, характеризующаяся микроорганизмами, присутствующими и (или) выделяемыми в ней. |
|
Ламинарный поток |
Однонаправленный поток воздуха, в котором скорости воздуха вдоль параллельных линий тока одинаковы. |
|
Другие производственные зоны |
Производственные зоны и помещения, не относящиеся к критическим производственным зонам, в которых продукция не открыта для контакта с окружающей средой. |
|
Квалификация оборудования |
Выполнение и документальное оформление проверок с целью доказательства того, что оборудование (производственное оборудование, измерительные приборы), используемые в производственном процессе, правильно выбраны, установлены и работают в соответствии с утвержденной документацией во всех предусмотренных режимах эксплуатации. |
|
Валидация процесса |
Проверка действием и подтверждение соответствия того, что документированная процедура, дающая высокую степень уверенности в том, что конкретный процесс, метод или система будет последовательно приводить к результатам, отвечающим заранее установленным критериям применяемости. |
|
Валидационный план |
Документ, который описывает философию, стратегию и методологию предприятия по проведению валидации. |
|
Валидационный протокол |
Документ, отражающий результаты валидации процессов и квалификации: проектной документации, монтажа, функционирования и эксплуатации оборудования, инженерных систем, «чистых» помещений и др. |
|
Квалификация |
Оценка и документированное подтверждение того, что проектная документация, оборудование инженерные системы и другие условия производства способны обеспечить достижение ожидаемых и воспроизводимых результатов. |
|
Критическая ситуация |
Условия или комплекс условий, относящийся к верхним и нижним пределам параметров технологического процесса и связанными с ними факторами, определенными инструкциями, которые могут привести к высокой вероятности брака в технологическом процессе или конечной продукции по сравнению с «идеальными» условиями. |
|
Технологический процесс |
Научно обоснованный комплекс действий, необходимых для получения готового продукта, он состоит из отдельных, следующих одна за одной стадий производства. |
|
Качество |
Совокупность свойств и характеристик продукта, которые влияют на его способность удовлетворять заявленные потребности. |
|
Квалификация функционирования |
Оценка и документированное подтверждение соответствия работоспособности технологического и лабораторного оборудования, инженерных систем, оснащенных «чистых» помещений и др. требованиям нормативной и технической документации. |
|
Квалификация эксплуатации |
Оценка и документированное подтверждение соответствия надежности и эффективности эксплуатационных параметров технологического оборудования, инженерных систем, функционирующих «чистых» помещений и др. требованиям нормативной и технической документации. |
|
Процесс |
Совокупность взаимосвязанных ресурсов и деятельности, которая преобразует входящие элементы и выходящие. |
|
Процедура |
Упорядоченная совокупность взаимосвязанных определенными отношениями действий, направленных на решение задач. |
|
Инициальная исходная (начальная) контаминация |
Загрязнение продукции в процессе производства, отбора проб, упаковки, хранения или внутрипроизводственной транспортировки. |
|
Класс чистоты производственного помещения |
Степень чистоты воздуха производственного помещения, характеризуемая содержанием механических частиц определенного размера и (или) жизнеспособных микроорганизмов в 1 м3 воздуха. |
|
Полупродукт |
Продукт на промежуточной стадии или на производственном этапе частичной готовности. |
|
Легализация |
Наличие соответствующих документов, иллюстрирующих высшую степень уверенности, что благодаря методам контроля, предприятие намерено и способно производить качественную продукцию. |
|
Санпропускник |
Специальное помещение при входе персонала в чистое производственное помещение, предназначенное для смены переходной одежды и обуви персонала на технологическую, представляющее собой замкнутое герметизированное пространство, отделенное дверьми от помещений. |
|
Тамбур-шлюз |
Специальное помещение, служащее для предотвращения поступления механических частиц и микроорганизмов при внесении продукции, материалов и оборудования в чистое производственное помещение. |
|
Воздушный шлюз |
Устройство, предназначенное для обдува персонала очищенным воздухом перед входом в чистое помещение. |
|
Переходная одежда |
Комплект спецодежды и обуви, который используется работающим персоналом вне чистых производственных помещений. |
|
Технологическая одежда |
Комплект спецодежды и обуви, используемый в чистых производственных помещениях и предназначенный для защиты изделий медицинского назначения, полупродуктов и вспомогательных материалов от вторичного загрязнения механическими частицами и микроорганизмами, выделяемыми персоналом. |
|
Готовая продукция |
Продукция, прошедшая все последовательные стадии технологического процесса, включая упаковку, маркировку, контроль качества, и готовая к реализации. |
|
Технологический операционный контроль |
Проверки, выполняемые в ходе производства с целью контроля и, в случае необходимости, корректировки параметров технологического процесса с тем, чтобы продукт соответствовал требованиям спецификации. Контроль за состоянием окружающей среды и (или) оборудования также рассматривается как элемент операционного контроля. |
|
Перекрестное загрязнение |
Загрязнение материалов или продукции другими материалами или продукцией. |
3. Персонал
3.1 Общие положения
3.1.1 Установление и поддержание удовлетворительной работы системы обеспечения качества, правильное изготовление и контроль медицинской продукции основывается на людских ресурсах. По этой причине для получения готовой продукции высокого качества, должен использоваться персонал соответствующей квалификации, обладающий практическим опытом
3.1.2 Весь персонал должен быть ознакомлен с основными положениями настоящих правил, относящихся к его производственной деятельности. Каждый сотрудник должен ясно представлять меру своей личной ответственности за качество, что должно быть отражено в должностных инструкциях предприятия.
3.1.3 Все сотрудники должны пройти начальное и последующее обучение основам «Правил...», включающих необходимые правила по личной гигиене.
3.1.4 Руководитель предприятия должен определить и документально оформить политику, задачи и обязательства в области качества. Политика в области качества должна быть согласована с организационными целями руководителя и ожиданиями и потребностями потребителей. Руководитель должен обеспечить понимание этой политики, ее проведение и поддержку на всех уровнях организации в соответствующих нормативных документах предприятия.
3.1.5 Руководитель предприятия должен анализировать систему качества через определенные интервалы времени, достаточные для того, чтобы обеспечить ее постоянную пригодность и эффективность действия, организацию реализации намеченной политики и задач в области качества.
3.2 Руководящий персонал
3.2.1 Руководитель предприятия должен иметь четкую организационную структуру. Служебные обязанности руководящих сотрудников должны быть четко определены, и эти лица должны обладать достаточными правами для реализации своих служебных полномочий. Не должно быть разрывов зон ответственности сотрудников. При необходимости может быть дублирование зон ответственности,
3.2.2 Проведение политики предприятия в области качества должны обеспечивать руководители, отвечающие за вопросы организации производства, контроля качества продукции, реализации продукции и другие ответственные специалисты.
Лица, ответственные за выполнение этих обязанностей, должны соответствовать квалификационным требованиям; функции руководителей должны быть четко определены во избежание дублирования и неопределенностей.
3.2.3 В обязанности руководителя производства должны входить:
- составление графиков производства;
- организация производства в соответствии с требованиями технологической документации и «Правил...» для получения готового продукта надлежащего качества;
- обеспечение процесса производства исходными материалами, сырьем;
- утверждение производственных инструкций, включая инструкцию по проведению постадийного контроля процесса производства, и обеспечение их точного соблюдения;
- подготовка и составление отчетов по изготовлению партий изделий;
- обеспечение правильного ведения текущей производственной документации (отчетов о партии, операционных карт и др.) и утверждение их ответственными сотрудниками перед передачей в отдел контроля качества;
- осуществление контроля за состоянием производственных помещений, оборудования и его техническим обслуживанием;
- обеспечение проведения валидации технологического оборудования, производственных процессов и проверки контрольно-измерительных приборов, хранения оригиналов документации и отчетов в доступной форме в определенном месте;
- контроль за проведением обучения персонала по утвержденным программам, как в начале, так и в ходе дальнейшей работы на предприятии;
- контроль качества продукции в процессе изготовления в соответствии с технологическим регламентом;
- обеспечение надлежащего движения материалов и изделий в пределах производственных помещений и хранения готовых изделий;
- обеспечение соблюдения персоналом правил техники безопасности и промышленной санитарии.
3.2.4 В обязанности руководителя отдела контроля качества должны входить:
- проведение входного контроля и выдача разрешения на использование в производстве исходного сырья, вспомогательных, упаковочных и маркированных материалов и полупродуктов, а также разрешение на реализацию готовой продукции;
- обеспечение составления и утверждение методик контроля и инструкций по проведению анализов сырья и материалов, полупродуктов и готовой продукции, инструкций по оценке и контролю условий производства и других документов, непосредственно связанных с контролем качества готовой продукции;
- организация и проведение контроля стадий и операций процесса производства в соответствии с технологическим регламентом производства продукции;
- участие в разработке маршрутных и операционных карт и процессов изготовления;
- контроль качества готовой продукции и выдача разрешения к ее реализации, а также контроль сохраняемости ее качества в течение гарантийных сроков годности;
- обеспечение проведения процессов валидации, включая валидацию методов контроля контрольно-измерительных приборов;
- хранение арбитражных образцов продукции и проведение контроля их в случае предъявления рекламаций на продукцию;
- хранение документации по результатам контроля продукции на всех стадиях процесса производства продукции, в том числе, и паспортов на реализованную продукцию;
- утверждение программ обучения персонала предприятия, в том числе, отдела контроля качества, и контроль за проведением обучения, как в начале, так и в ходе дальнейшей работы.
3.2.5 Руководитель отдела контроля качества может выполнять функции Уполномоченного лица при экспорте продукции.
Руководитель производства и руководитель отдела контроля качества, кроме того, совместно должны отвечать за:
- контроль за соблюдением требований «Правил...»;
- составление и утверждение технологических регламентов и другой текущей производственной документации, включая дополнения и изменения к ним;
- контроль за соблюдением на производстве соответствующих санитарно-гигиенических норм;
- проведение самоинспекции;
- контроль и принятие мер по рекламациям на продукцию.
3.3 Обучение персонала
3.3.1 К работе на производственных участках чистых (асептических) производств полимерных изделий, тканых и нетканых материалов, контактирующих с кровью должны допускаться лица не моложе 18 лет, имеющие соответствующую квалификацию, обладающие необходимым объемом теоретических знаний и практических навыков для работы на указанных производствах.
3.3.2 Перед началом работы вновь поступивший персонал должен пройти профессиональное и производственное обучение, медицинское обследование, вводный и первичный инструктаж по безопасности труда на рабочем месте с оформлением в журнале регистрации в соответствии с ГОСТ 12.0.004.
3.3.3 Обучение должно проводиться на основании плана обучения и программ, утвержденных руководством предприятия или начальниками производственных участков или руководителем отдела контроля качества.
3.3.4 Все занятия должны протоколироваться в регистрационных журналах. Протоколы, содержащие сведения о прохождении обучения каждым сотрудником в течение всего времени его работы на производстве, должны храниться на предприятии.
3.3.5 Обучение, инструктаж и обследование должны проводиться в соответствии с разработанными и утвержденными руководством предприятия правилами или инструкциями по:
- обучению теоретическим знаниям и практическим навыкам работы на конкретном производственном участке;
- технике безопасности и охране труда (кроме основных сведений в документе должны быть оговорены правила поведения персонала в аварийных ситуациях - при аварийном отключении электроэнергии, пожаре и др.);
- поведению и работе на асептических производствах (личной гигиене, асептической техники, подготовке к работе, поведению во время и после работы, порядку смены одежды и переодевания перед входом в асептическую зону и др.);
В документе обязательно должен быть оговорен вид загрязнений и микроорганизмов, к которым наиболее чувствительна производимая продукция, а также указаны меры по минимизации и контролю этих загрязнений и микроорганизмов;
- медицинскому освидетельствованию (в документе должны быть регламентированы медицинские критерии оценки состояния здоровья служащих для установления пригодности персонала к работе на данном участке - отсутствие у работающих в зонах асептических производств аллергических, кожных, инфекционных заболеваний, патогенной микрофлоры, открытых ран и повреждений на коже и других заболеваний и нарушений состояния здоровья, которые могут послужить причиной попадания загрязнения в готовую продукцию и оказать нежелательное воздействие на ее качество).
3.3.6 Сведения, излагаемые в правилах и инструкциях, должны соответствовать современному научно-техническому уровню.
При необходимости замены устаревших сведений, введения новшеств и уточнений, внесения изменений в производственный процесс указанные документы должны корректироваться.
3.3.7 К самостоятельной работе должен допускаться персонал, аттестованный на право работать на соответствующем участке асептического производства (успешно прошедший обучение, инструктаж и получивший положительное заключение о состоянии здоровья и пригодности для работы на данном участке).
3.3.8 В процессе работы весь персонал должен регулярно проходить переподготовку и переаттестацию (не реже 1 раза в год), повторные инструктажи по безопасности труда на рабочем месте с оформлением в журнале регистрации (не реже одного раза в шесть месяцев) и медицинские обследования (не реже 1 раза в год).
3.3.9 Персонал, обслуживающий оборудование и приборы (осуществляющий монтаж и ремонт) и занимающийся уборкой в асептических помещениях, также должен быть аттестован на пригодность к работе в асептических зонах.
3.4 Условия работы в чистых помещениях, защитная одежда персонала, гигиена персонала
3.4.1 Особое внимание должно уделяться подготовке персонала, работающего в чистых помещениях, включая персонал, занятый обслуживанием и ремонтом оборудования, подготовкой помещений к работе и т.п. Персонал должен обладать знаниями и опытом, необходимым для производства медицинских изделий из полимерных материалов, в том числе, по гигиене и микробиологии.
3.4.2 Персонал, занятый в процессе производства на упаковке и хранении медицинских изделий из полимерных, тканых и нетканых материалов, должен соблюдать инструкции, регламентирующие состояние здоровья и требования гигиены.
3.4.3 При поступлении на работу персонал должен пройти медицинское обследование. Весь персонал, занятый непосредственно на производстве, включая временно работающих, должен проходить регулярные медицинские осмотры. Персонал, осуществляющий визуальный контроль, должен проходить регулярные осмотры врачами-окулистами.
3.4.4 К работе, связанной с изготовлением изделий медицинского назначения, не должны допускаться сотрудники с инфекционными заболеваниями, открытыми ранами на коже и носители патогенной микрофлоры, пока их состояние не нормализуется.
3.4.5 Персонал должен ставить в известность своего руководителя о любых недомоганиях (кожные заболевания, острые респираторные заболевания и др.), способных оказать нежелательные воздействия на продукцию.
3.4.6 Виды косметики, содержащие частицы, например, пудра, лаки для волос и для ногтей, не допускаются для работников в чистых помещениях. Личные вещи персонала - кошельки, сумки, легко снимаемые ювелирные изделия, должны содержаться в комнатах для переодевания.
3.4.7 Запрещается есть и курить, а также хранить еду, курительные материалы, в производственных помещениях и на складах.
3.4.8 Каждый человек, входящий в производственные помещения, должен быть одет в специальную одежду, соответствующую выполняемым им производственным операциям.
3.4.9 Работающие в чистых помещениях обязаны:
- строго ограничить вход в чистые помещения и выход из них, для чего должны быть разработаны соответствующие инструкции;
- осуществлять производственный процесс минимально необходимым количеством персонала. Инспекционные и контрольные процедуры, в основном, следует проводить за пределами чистых зон;
- ограничить перемещения в помещениях классов чистоты А, В и С (таблица 1). Избегать резких движений в помещениях класса А;
- не поднимать и не использовать предметы, упавшие на пол во время работы;
- избегать разговоров на посторонние темы;
- перед входом в чистые помещения (в помещении санпропускника) снять все украшения и удалить косметику, включая лак для ногтей, принять душ и вымыть руки щеткой с моющими средствами; обработать руки дезинфицирующими средствами, переодеться из переходной одежды и обуви в технологическую одежду и обувь.
3.4.10 Правила, порядок входа в помещения и поведения в чистой комнате и контролируемой зоне должны выполняться ВСЕМ персоналом, включая посетителей, ремонтных рабочих и рабочих по уборке помещений и оборудования.
Необязательный персонал и посетители не должны допускаться в эти помещения.
3.4.11 Посещение производственных участков посторонними лицами осуществляется только с разрешения начальника цеха. Для этого в санпропускнике должны быть запасные комплекты спецодежды.
Ни одно лицо не может пройти в помещение, минуя комнату для переодевания, где должна быть оставлена верхняя одежда.
Все лица должны вымыть руки сразу после того, как одета специальная одежда, ее не должны носить за пределами чистой комнаты или контролируемых чистых помещений.
3.4.12 Сотрудники, работающие в чистых помещениях, должны знать и использовать форму специальной одежды для работы в помещениях различных классов чистоты. Защитная одежда, предоставляемая персоналу и посетителям, должна быть изготовлена из безворсового материала и должна полностью закрывать человека и его повседневную одежду. Форма одежды для помещений класса чистоты D должна быть следующая: комбинезон или куртка и брюки или халат; шапочка или косынка из хлопчатобумажных или льняных тканей; соответствующая обувь или бахилы, одеваемые сверху на обувь.
Форма одежды для помещений класса чистоты В и С должна быть: комбинезон или куртка и брюки (рукава собраны на запястьях, воротник выполнен в виде высокой стойки); шапочка или косынка; соответствующая обувь или бахилы; при необходимости, маска.
Форма одежды для помещений класса чистоты А должна быть: комбинезон с воротником-стойкой, стянутый на поясе, без карманов, с манжетами, плотно облегающими кисти рук, и с защипами, плотно облегающими щиколотки ног; головной убор в виде шлема-капюшона, полностью закрывающих волосы, нос, рот и подбородок; стерильные перчатки из резины или эластичных полимеров; простерилизованная или продезинфицированная обувь с одетыми сверху бахилами, полностью закрывающими ступню (нижняя часть брюк должна быть заправлена в бахилы, рукава комбинезона - в перчатки, ни одна часть тела или нижнего белья не должна быть открыта).
3.4.13 Одежда должна застегиваться по всей длине, около шеи и запястий. Одежда должна легко одеваться.
Головные уборы должны полностью закрывать волосы; руководитель должен следить за тем, что они надеты правильно. Работающим в чистых помещениях людям не разрешается носить бороды и усы.
Обувь должна быть из неволокнистого материала и должна постоянно подвергаться очистке. Возможно использование одноразовой обуви.
Если работники работают в перчатках, то в этом случае перчатки должны быть сделаны из безворсового и не впитывающего материала. Каждый раз после выхода из стерильного помещения перчатки должны заменяться на новые.
Спецодежда должна храниться отдельно от повседневной верхней одежды и должна сохраняться в чистом виде. Для каждого типа помещений и типа проводимых работ должна быть своя спецодежда.
3.4.14 Технологическая одежда для работы в помещениях А, В, С, D классов чистоты должна быть изготовлена из ткани, удовлетворяющей следующим требованиям:
- ворсоотделение - не более 8 частиц размером свыше 1 мкм/см;
- электрический заряд - 0;
- плотность: по основе - 370, по утку - 316;
- воздухопроницаемость не ниже 300 м2/м2 с;
- гигроскопичность не менее 7 %.
Технологическая одежда может быть однократного и многократного использования. В первом случае каждому вновь входящему в чистую зону следует выдавать новый комплект. Если одежда предназначена для многократного пользования, то при каждом входе на участок в зависимости от класса чистоты помещения и в соответствии с инструкциями о периодичности смены спецодежды выдается свежевыстиранный или стерильный комплект.
3.4.15 Одежду необходимо стирать таким образом, чтобы она не подвергалась дополнительному загрязнению. На предприятии необходимо иметь специализированную прачечную.
Стирку одежды следует проводить в изолированном чистом помещении. Одежду в помещение стирки следует привозить в закрытых крышками баках. Перед стиркой технологическая одежда подлежит осмотру с целью установления необходимости ремонта и степени износа.
Стирку нужно производить с разделением одежды по цветам и принадлежностям.
Сушку одежды следует производить в отдельном помещении. Высушенная и выглаженная одежда при необходимости упаковывается в биксы и направляется на стерилизацию. Персонал, осуществляющий сушку и упаковку технологической одежды, должен работать в технологической одежде из безворсовой ткани.
Для определения пригодности технологической одежды к дальнейшему использованию необходимо ворсоотделение ткани проверять после каждой обработки.
3.4.16 Стерилизацию технологической одежды и перчаток следует проводить в автоклавах проходного типа. После истечения времени стерилизации необходимо подсушить стерилизуемый материал под вакуумом и охладить стерильным обеспыленным воздухом. Выгрузка стерильного материала производится в чистое помещение.
3.4.17 Чистая или стерильная одежда и перчатки должны храниться в условиях, предотвращающих их загрязнение.
Передача технологической одежды в помещение подготовки персонала (санпропускник технологической одежды) должна осуществляться через воздушный шлюз.
Спецобувь должна храниться в шкафу, оборудованном бактерицидными лампами.
При работе, как в перчатках, так и без них, руки следует обрабатывать дезинфицирующими средствами в соответствии с инструкциями (например, раствором диоцида 1:3000, 1:5000 и рецептурой С-4); для сушки рук после их обработки используют электросушилки с подачей воздуха из чистого помещения.
3.4.18 Порядок подготовки персонала в чистых помещениях изложен в приложении.
3.4.19 На предприятии должны действовать инструкции, устанавливающие:
- порядок проведения медицинских осмотров персонала;
- правила соблюдения личной и производственной гигиены персонала;
- порядок подготовки персонала к работе;
- правила приготовления растворов дезинфицирующих средств для обработки перчаток и рук персонала;
- порядок мойки рук и обработки перчаток и рук дезинфицирующими средствами;
- порядок проведения контроля степени микробной контаминации рук персонала, перчаток;
- порядок проведения стирки и стерилизации технологической одежды.
Эти инструкции постоянно доводят до сведения соответствующего персонала и включают в программу подготовки и повышения квалификации.
4. Здания и рабочие помещения
4.1 Общие положения. Требования к генплану и окружающей территории. Классификация помещений
4.1.1 К производству стерильных изделий медицинского назначения из полимеров, тканых и нетканых материалов, имеющих контакт с кровью, предъявляются особые требования, которые вызваны необходимостью свести до минимума риск загрязнения микроорганизмами, частицами и пирогенами. Это во многом зависит от опыта персонала, его подготовки и отношения к работе. Исключительно важное значение имеет гарантия качества. Этот вид производства требует строгого выполнения методов подготовки и выполнения технологических процессов, которые должны быть тщательно отработаны и валидированы. Никакой процесс завершающей стадии производства или контроль качества готового изделия не могут рассматриваться как единственное средство обеспечения стерильности или других показателей качества изделия.
4.1.2 Здания и помещения должны быть расположены, спроектированы, построены и должны содержаться таким образом, чтобы они были пригодны для проведения соответствующих производственных операций, а также позволяли исключить возможность возникновения производственных ошибок. Подготовка помещений к работе и содержание их должны позволять устранять отрицательные воздействия на качество готового изделия: перекрестную контаминацию, скопление пыли и других загрязнений.
4.1.3 Площадки для нового строительства предприятий, как правило, следует выбирать вне промышленных зон и промузлов на территориях, наименее подверженных различным загрязнениям атмосферного воздуха. При этом площадка должна быть удалена от заводов ферментной и гидролизно-дрожжевой промышленности, предприятий белково-витаминного концентрата, антибиотиков, бактериальных препаратов, животноводческих и птицеводческих производственных помещений, молокозаводов, мясокомбинатов, очистных сооружений и т.п.
4.1.4 Предприятие по изготовлению стерильных изделий медицинского назначения должно располагаться в одном или нескольких производственных зданиях, размер, конструкция и расположение которых обеспечивают рациональное осуществление необходимого процесса производства.
4.1.5 Производственные здания, сооружения и помещения следует проектировать в соответствии с действующими строительными нормами, правилами и требованиями инструкции по строительному проектированию предприятий медицинской промышленности и настоящего документа.
4.1.6 Производственные здания должны быть спроектированы и построены таким образом, чтобы свести к минимуму запыление, загрязнение и исключить проникновение в них насекомых и животных. Здания должны быть сориентированы по сторонам света с учетом розы ветров таким образом, чтобы снизить инсоляцию чистых помещений и уменьшить ветровое давление на их наружные стены.
4.1.7 Планировка производственных зданий должна обеспечивать:
- поточность процесса с кратчайшими расстояниями между технологически связанными помещениями;
- исключить пересечение людских и технологических потоков;
- максимальную группировку помещений с одинаковой степенью чистоты;
- полное соблюдение условий санитарно-гигиенического режима;
- защиту от загрязнений при перемещении исходного сырья, деталей, узлов и изделий внутри зданий и из одного здания в другое;
- соблюдение норм и правил техники безопасности и пожарной безопасности.
4.1.8 В зданиях должны иметься:
- системы вентиляции, водопровода и канализации, удаления отходов производства и другие системы, необходимые для обеспечения чистоты помещений, оборудования, деталей, полуфабрикатов и готовых изделий;
- установки, необходимые для поддержания в помещениях температуры и относительной влажности воздуха, требуемых для сохранения качества изделий, узлов и изделий в процессе их изготовления, для обеспечения гигиенических требований к персоналу и надлежащей эксплуатации и четкости работы используемого оборудования;
- чистые и удобные санитарно-бытовые помещения, расположенные вблизи производственных помещений.
4.1.9. Помещения (включая производственные, складские и санитарно-бытовые) должны быть объединены в функционально-технологические блоки, предпочтительно с автономными системами инженерного обеспечения.
Производство стерильных изделий медицинского назначения должно выполняться в чистых зонах, доступ в которые персонала и (или) оборудования и материалов должен происходить через воздушные шлюзы. В чистых зонах должна поддерживаться чистота по соответствующему стандарту. Подаваемый воздух должен проходить через фильтры соответствующей эффективности.
4.1.10. Проектирование и строительство чистых помещений должно проводиться в соответствии с ГОСТами Р ИСО 14644.
4.2 Классификация помещений
4.2.1 Чистые зоны для производства стерильных изделий классифицируются в соответствии с требуемыми характеристиками окружающей среды. Каждый производственный процесс требует определенного уровня чистоты окружающей среды в функционирующем состоянии («в эксплуатации») с тем, чтобы минимизировать риск загрязнения продукта или используемых материалов частицами или микроорганизмами
Для того, чтобы соответствовать требуемым условиям в функционирующем состоянии («в эксплуатации»), эти зоны должны проектироваться так, чтобы обеспечить заданный класс чистоты воздуха в «оснащенном» состоянии.
При производстве стерильных изделий медицинского назначения предусматривается классификация чистых помещений и (или) зон по допустимому содержанию механических частиц в воздухе при двух состояниях - оснащенном и функционирующем, а также по допустимому содержанию колониеобразующих микроорганизмов в воздухе в функционирующем состоянии.
Под оснащенным состоянием подразумевается, что все системы чистого помещения и технологическое оборудование установлено и работоспособно, однако персонал в рабочей зоне отсутствует. Под функционирующим состоянием подразумевается, что все системы чистого помещения и технологическое оборудование находятся в рабочем состоянии в режимах, соответствующих требованиям регламента, а также в присутствии необходимого количества персонала, выполняющего свои производственные функции.
4.2.2 Для производства стерильных изделий медицинского назначения можно выделить четыре типа зон:
тип А: локальные зоны для операций с высокой степенью риска, например, зона системы приготовления и розлива консерванта при заполнении контейнеров полимерных для крови. Помещения должны обеспечиваться рабочей зоной с ламинарным потоком воздуха. Системы ламинарного потока воздуха должны обеспечивать однородную скорость воздуха 0,45 м/с ± 20 % (значение для руководства) в рабочем состоянии.
Тин В: для случая асептической подготовки и наполнения - пространство, окружающее зону типа А.
Типы С и Д: чистые зоны для выполнения менее ответственных этапов производства стерильных изделий (литье, экструзия, сборка, сварка, упаковка).
4.2.3 Классификация помещений для производства изделий медицинского назначения из полимеров, тканых и нетканых материалов приведена в таблице 1.
Таблица 1
|
В «оснащенном» состоянии (b) |
В «функционирующем» состоянии («в эксплуатации») |
Мах допустимое кол-во жизнеспособных микроорганизмов в 1 м3 воздуха |
|||
|
Максимально допустимое число частиц в 1 м3 воздуха, большее или равное |
|||||
|
0,5 мкм |
5 мкм |
0,5 мкм |
5 мкм |
||
|
А |
3500 |
0 |
3500 |
0 |
Менее 1 |
|
В (1) |
3500 |
0 |
350000 |
2500 |
10 |
|
С (1) |
350000 |
2000 |
3500000 |
20000 |
100 4) |
|
D (l) |
3500000 |
20000 |
Не определено 3) |
Не определено 3) |
200-500 4) 5) |
Примечания.
1) В зонах типов В, С и D кратность воздухообмена должна определяться с учетом размера помещения, находящегося в нем оборудования и персонала. Для зон типов А, В и С система снабжения воздухом должна иметь соответствующие фильтры, такие как НЕРА-фильтры.
2) Значения максимально допустимого числа аэрозольных частиц в «оснащенном» состоянии соответствуют классификации по федеральному стандарту США 209 Б и классификации ISO, ГОСТ Р 50766-95
типы А и В соответствуют классу 100; М 3,5; ISO 5; Р5 (100);
тип С соответствует классу 10.000, М 5,5; ISO 7; Р7 (10000);
тип D соответствует классу 100.000; М 6,5; ISO 8 (100000).
3) Требования и нормы зависят от вида готового продукта и характера выполняемых операций.
4) Производство нестерильных изделий медицинского назначения должно осуществляться в помещениях классов чистоты С и D. При этом предусматривается нормирование содержания жизнеспособных микроорганизмов в воздухе. Нормирование содержания механических частиц, как правило, не предусматривается.
4.2.4 Не допускается примыкание помещений классов чистоты В, С и D к наружным ограждающим конструкциям (стены помещений категории А и В по противопожарным нормам не должны быть капитальными). Помещения более высокого класса чистоты необходимо располагать внутри помещений более низкого класса
4.2.5 Помещения классов чистоты В, С и D запрещается располагать в подвале или в цокольном этаже.
4.2.6 Рекомендуемая классификация участков производства изделий медицинского назначения приведена в таблице 2.
Таблица 2
|
Наименование участков производства или операции |
|
|
Производство устройств инфузионных, трансфузионных и эксфузионных однократного применения |
|
|
D (c зонами С при выгрузке изделий) |
Участок подготовки сырья и материалов. Участок изготовления деталей методом литья под давлением (в т. ч участок литья капельницы). Участок экструзии трубки. Участок резки резиновых трубок. Участок сварки пакетов. Участок мойки игл. |
|
С |
Участок изготовления фильтра воздушного. Участок раскроя, вырезки и сварки фильтра. Участок мойки и сушки специальных и резиновых трубок. Участок ультразвуковой сварки капельницы (в т.ч. с иглой полимерной). Участок сварки и упаковки устройств. Участок запрессовки игл. |
|
Производство контейнеров инфузионных и контейнеров для крови и ее компонентов однократного применения |
|
|
С (с зоной класса А) |
Розлив консерванта |
|
С |
Участок подготовки игл. Участок предварительной сборки деталей контейнеров. Участок сборки и высокочастотная сварка деталей. Приготовление консерванта. |
|
С (с зоной А и В) |
Участок паровой стерилизации. (Чистая сторона) Участок газовой стерилизации. (Чистая сторона) Участок индивидуальной упаковки изделий. |
|
D (с зонами С при выгрузке изделий) |
Участок изготовления деталей методом литья под давлением. Участок экструзии пленки. Участок экструзии трубок. Участок групповой упаковки. Участок мойки игл. |
|
Производство гемодиализаторов |
|
|
С |
Участок подготовки комплектующих и комплектование. Участок сборки гемодиализаторов. Участок упаковки в индивидуальную тару. |
|
D |
Участок изготовления деталей методом литья под давлением. Участок экструзии. Участок изготовления пакетов, нанесение печати. |
|
Производство шприцев однократного применения |
|
|
С |
Участок нанесения печати. Участок индивидуальной упаковки. |
|
D (с зонами С при выгрузке изделий) |
Участок подготовки сырья и материалов. Участок изготовления деталей методом литья под давлением. Участок сборки шприцев. Газовая стерилизация шприцев. |
|
Производство игольных заготовок и игл инъекционных |
|
|
С |
Участок сборки игл. Участок упаковки игл. |
|
D (с зонами С) |
Участок подготовки сырья и материалов. Участок изготовления трубки. Участок мойки и сушки игл. Участок изготовления деталей методом литья под давлением. Участок газовой стерилизации. |
|
Производство катетеров, трубок и магистралей |
|
|
С |
Участок подготовки сырья и материалов. Участок формирования деталей из пластизоля. Участок сборки. Участок упаковки в индивидуальную тару. |
|
D (с зонами С при выгрузке изделий) |
Участок изготовления деталей методом литья под давлением. Участок экструзии трубок. Участок упаковки в групповую тару. |
|
Производство изделий «Пленки операционные липкие полимерные ЛПО» |
|
|
D |
Изготовление рулонного липкого ламината. Активация поверхности пленки. Нанесение адгезива на пленку-основу. Сушка клеевого покрытия при температуре (50 - 70) °С. Ламинирование (покрытие литой пленки защитным покрытием из антиадгезионной бумаги). Резка полотна. Изготовление пакетов индивидуальной упаковки. Упаковка в индивидуальные пакеты и нанесение печати. Радиационная стерилизация. |
|
Производство вязаных фильтров и сосудов для крови, полотен и сетчатых эластичных бинтов |
|
|
D |
Изготовление полотен на плетельных машинах и лентоткацких станках. |
|
Изготовление трикотажных полотен и вязание фильтров на круглотрикотажных основовязальных машинах. |
|
|
Изготовление бинтов и протезов на плоскофанговых машинах. |
|
|
Стирка, обработка и промывка полотен и трикотажных трубок. |
|
|
Сушка полотен и трикотажных трубок. |
|
|
Термическая обработка полотен и трикотажных трубок. |
|
|
D (с зоной выгрузки С) |
Вторичная стирка готовой продукции. |
|
С |
Упаковка продукции. |
|
D |
Стерилизация. |
|
Производство салфеток кровоостанавливающих «Колитекс-ген», салфеток «Асептика», бинтов липких проницаемых (на основе нетканых материалов) |
|
|
С |
Приготовление адгезива с лекарственными средствами. |
|
D |
Изготовление рулонного ламината. |
|
Нанесение адгезива на нетканый материал. |
|
|
Сушка материала. |
|
|
Охлаждение материала. |
|
|
D (с зоной С) |
Резка и дублирование. |
|
С |
Упаковка в индивидуальную тару. |
|
D |
Упаковка в транспортную тару. |
|
Производство мембран для тонкой очистки и стерилизации препаратов крови. |
|
|
С |
Зона формования пористой пленки. Сушка пористой пленки. Нарезка фильтроэлементов и прокладок. Первичная упаковка. |
|
D (с зоной выгрузки С) |
Промывка пористой пленки. |
|
D |
Подготовка сырья и материалов. Приготовление формовочного раствора. Вторичная упаковка |
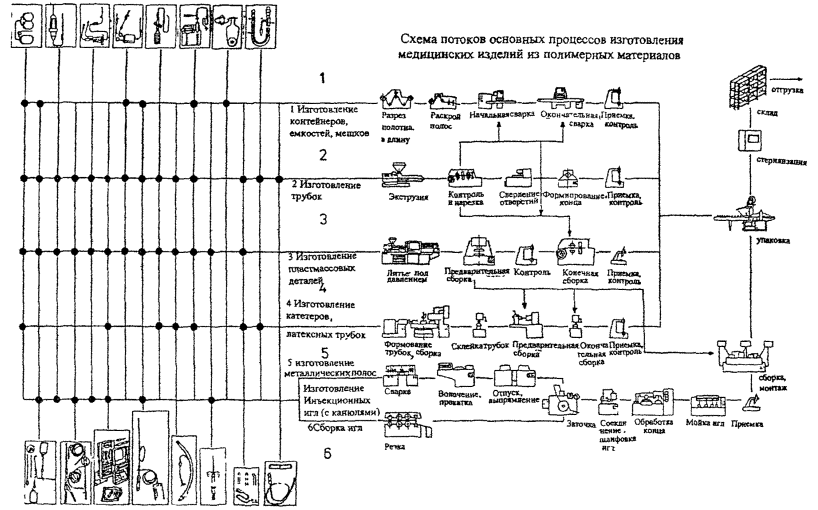
Потоки основных процессов изготовления медицинских изделий из полимерных материалов, тканых и нетканых материалов медицинского назначения, имеющих контакт с кровью, представлены на схемах 1 и 2 (Приложение 1 и 2).
4.3 Конструктивные особенности помещений
4.3.1 Помещения для производства и контроля качества изделий медицинского назначения, а также упаковки их в потребительскую тару:
- должны быть достаточно просторными и оборудованы таким образом, чтобы правильно организовать технологический процесс, не загромождать проходы для перемещения материалов и персонала, исключить возможность перекрестного загрязнения, смешивания отходов и брака с готовыми деталями и узлами;
- должны быть оборудованы местными отсосами для удаления пыли и вредных веществ в местах их образования (например, продуктов деструкции полимера при литье, экструзии, сварке, паров растворителей и т.д.);
- должны иметь гладкие бесшовные внутренние поверхности (стены, полы, потолки, двери) с минимальным количеством выступающих частей и ниш, должны быть непроницаемыми для жидкостей и легко доступными для мытья и обработки дезинфицирующими средствами. Материалы, применяемые при отделке производственных помещений должны быть непылящими, непористыми, легко моющимися, влагостойкими, антистатическими, негорючими и устойчивыми к воздействию дезинфицирующих средств;
- в помещениях классов чистоты В и С не допускается закрытая прокладка коммуникаций и воздуховодов; подводку коммуникаций к оборудованию следует осуществлять вертикальными участками из технических этажей и полов и выполнять из материала, стойкого к воздействию дезинфицирующих веществ;
- сопряжения между стенами, полами и потолками желательно иметь закругленной формы (для помещений класса А обязательно);
- должны содержать минимально необходимое для ведения производственного процесса количество оборудования и мебели; материалы, из которых изготовлена мебель, должны быть легко моющимися и устойчивыми к воздействию дезинфицирующих средств. Следует избегать деревянных поверхностей, использование неокрашенных деревянных поверхностей недопустимо;
- подвесные потолки в помещениях должны быть тщательно загерметизированы для предотвращения выделения пыли из пространства над ними;
- для обеспечения надежной герметизации стыков всех конструктивных элементов в помещениях должны применяться упругие прокладки и строительные герметики;
- фильтры тонкой очистки воздуха должны быть тщательно загерметизированы и расположены в месте подачи воздуха в чистое помещение или как можно ближе к нему;
- не допускается использование скользящих дверей;
- ленты транспортеров могут проходить сквозь стены чистых помещений одного класса чистоты;
- между помещениями различных классов чистоты желательно иметь электромеханические переговорные устройства;
- давление в помещениях классов чистоты А, В и С должны быть выше, чем в близлежащих помещениях;
- использование раковин и сливных труб в различных производственных помещениях классов чистоты А, В и С должно быть исключено, а в помещениях класса D - желательно исключить. Если же это невозможно, сливные трубы должны быть легко доступны для мытья и обработки, снабжены устройствами для предотвращения попадания в водопроводную сеть воды из канализации;
- производственные помещения не должны использоваться для проведения контроля стерильности и других микробиологических анализов. Помещения лабораторий для контроля стерильности, микробиологических анализов и др. должны быть изолированы, располагаться отдельно от производственных помещений и оборудованы в соответствии с действующими для них нормами;
- вход персонала и передача материалов в чистые помещения должны осуществляться через воздушные шлюзы, в которых осуществляется интенсивный обдув и очистка направленным сверху вниз очищенным воздухом. Не допускается одновременное открытие дверей в шлюзе; двери должны быть самозакрывающимися с уплотненным притвором;
- помещения должны содержаться в безупречной чистоте, подвергаясь обязательной ежедневной и генеральной уборке и периодическому ремонту;
- помещения могут подвергаться УФ-облучению для обеззараживания воздуха с помощью стационарных или переносных облучателей (в отсутствии людей);
- должны иметь температурный режим, влажность воздуха и вентиляцию, не оказывающие прямого или косвенного отрицательного воздействия на качество деталей, узлов, готовых изделий во время их производства, а также на функционирование оборудования; освещение должно быть достаточным для контроля за работой оборудования и за качеством изготавливаемых деталей;
- помещения для производства и контроля качества изделий медицинского назначения не должны использоваться для других целей.
4.3.2 Помещения для упаковки изделий медицинского назначения во вторичную, групповую, транспортную тару должны:
- быть достаточно просторными, чтобы можно было правильно организовать технологические операции и не загромождать проходы для перемещения материалов;
- иметь освещение и параметры воздушной среды, не оказывающие отрицательного влияния на функционирование оборудования, а также на качество упаковки и качество упаковываемого изделия;
- иметь такое расположение оборудования, чтобы исключить возможность смешивания изделий (недопустимо упаковывать рядом изделия, имеющие сходный внешний вид).
4.3.3 Помещения для хранения сырья, вспомогательных и упаковочных материалов, готовой продукции должны;
- быть достаточно просторными, чтобы обеспечить упорядоченное и раздельное хранение исходного сырья, вспомогательных, упаковочных материалов, карантинное хранение готовых изделий, хранение забракованных изделий и возвратных отходов;
- обеспечивать надежную защиту от случайного или злоумышленного загрязнения или заражения;
- отвечать действующим правилам хранения и обращения с воспламеняющимися и взрывчатыми продуктами производства, токсическими веществами;
- быть чистыми, сухими и иметь необходимое освещение, вентиляцию, температуру и влажность воздуха.
Вход в помещения хранения разрешается только персоналу, имеющему соответствующие полномочия.
Вместимость цехового склада должна быть такой, чтобы обеспечить бесперебойную работу в течение недели.
В состав производственных участков должны входить промежуточные склады для хранения деталей, узлов и полуфабрикатов.
Промежуточные склады должны быть оборудованы постоянно горящими бактерицидными лампами.
Производственный процесс должен быть организован таким образом, чтобы срок хранения деталей, узлов и т.п. на промежуточном складе составлял не более 3-х дней.
4.3.4 Состав санитарно-бытовых помещений должен определяться характером производственных процессов.
Для хранения одежды различных видов (уличной, повседневной и специальной одежды - переходной и технологической) должны быть предусмотрены гардеробные. Гардеробные для хранения уличной, повседневной и переходной одежды должны располагаться при входе в здание. Технологическая одежда должна храниться в специальных гардеробных в санпропускниках.
Душевые, помещения для мытья рук и туалеты должны быть изолированы от производственных и складских помещений, но расположены вблизи от производственных помещений.
Помещения для приема пищи и отдыха должны быть изолированы от других помещений
4.3.5 Вход в производственные помещения классов чистоты А, В, С, D должен быть организован через санпропускники (отдельно для каждого пола работающих) с надлежащей вентиляцией и соответствующим оборудованием, и воздушными шлюзами.
Санпропускники должны быть сконструированы и использованы таким образом, чтобы обеспечить разделение различных этапов переодевания и обработки рук и тем самым свести к минимуму возможность загрязнения технологической одежды микроорганизмами и механическими частицами. В эти помещения можно входить лишь в чистой переходной одежде и сменной обуви.
Санпропускники должны располагаться вне зоны производства медицинских изделий, непосредственно прилегая к производственным чистым помещениям.
Санпропускники должны быть оборудованы:
- умывальниками с холодной и горячей водой; для помещений класса А умывальники должны быть с управлением с помощью локтя или ноги;
- воздушными сушилками для рук;
- вешалками для переходной спецодежды;
- вешалками для технологической спецодежды;
- зеркалами для контроля правильности одевания косынок или шапочек;
- шкафами, оборудованными постоянно или периодически горящими бактерицидными лампами, для хранения спецобуви.
Кроме того, в помещениях должны находиться закрывающиеся емкости для использованной технологической одежды, а также моющие и дезинфицирующие средства для мытья и обработки рук.
4.3.6 Требования к отделке чистых помещений.
Ограждающие конструкции здания должны быть герметичными, не пылящими и снижающими влияние внешних атмосферных условий на микроклимат чистых помещений, а также позволяющими проводить влажную уборку.
Материалы, применяемые в отделке помещений должны соответствовать следующим требованиям:
- обладать достаточной механической прочностью, относительно небольшим водопоглощением, не поддаваться коррозии, негорючими и долговечными;
- нетоксичными, обладать бактерицидностью, пылеотталкивающей способностью, ограниченной статической электризацией;
- обладать соответствующими декоративно-художественными качествами.
Материалы для стен, потолка и пола не должны осыпаться, крошиться, не выделять пыли и легко чиститься, допускать влажную уборку дезинфицирующими растворами.
Стены, потолки, двери должны быть ровными, гладкими, без трещин, иметь как можно меньше углублений, карманов и горизонтальных поверхностей, способствующих образованию и оседанию пыли, отделка - из пылеотталкивающих материалов. Не допускается отслаивание и шелушение отделочных материалов.
Стены и перегородки допускается изготавливать из стекло-алюминиевых панелей, стеклоблоков и других индустриальных материалов, щели и швы следует герметизировать тиоколовыми мастиками или применять неосыпающиеся связующие растворы и шпатлевочные составы.
4.3.7 Полы должны быть гладкими, не собирающими пыли, легко поддающимися влажной уборке, прочными, гигиеничными с минимальным количеством швов.
4.3.8 Соединения элементов ограждающих конструкций (потолка, стен, перегородок, остекления) должны предусматривать возможность проведения влажной уборки. Переход от стен к полу и потолку, а также стыки стен рекомендуется выполнять с закруглением, равным 1300 мм.
Алюминиевые листы, применяемые для изготовления элементов чистых помещений, должны быть анодированы с целью исключения коррозии и увеличения долговечности в условиях применения во время влажных уборок дезинфицирующих растворов.
4.3.9 Подготовительные работы и отделка поверхностей помещений должны выполняться высококачественно. Стыки элементов конструкций и места пропуска инженерных сетей необходимо уплотнять.
4.3.10 Вспомогательные помещения (кладовые приготовления дезрастворов, помещения обработки тары, перемотки рулонных материалов и т.п.), пространство за подвесным потолком и технические этажи, примыкающие к чистым помещениям, следует отделывать материалами, обеспечивающими устойчивую глянцевую поверхность и легкую очистку и уборку.
4.4 Отопление. Вентиляция. Кондиционирование
4.4.1 Отопление, вентиляцию и кондиционирование в производственных зданиях следует проектировать в соответствии с действующими строительными нормами и правилами и требованиями инструкции по строительному проектированию предприятий медицинской промышленности и настоящего документа.
4.4.2 Производительность приточных систем вентиляции и кондиционирования воздуха следует определять, исходя из условий обеспечения требуемых параметров воздуха в рабочей зоне с учетом принятой схемы организации воздухообмена и класса чистоты помещения.
Воздухозаборные устройства приточной вентиляции следует располагать в местах с максимальной чистотой воздуха с учетом направления господствующих ветров.
4.4.3 Очистка приточного воздуха, подаваемого в помещениях классов чистоты А, В и С должна быть трехступенчатой.
Очистка приточного воздуха, подаваемого в помещения класса чистоты D, может быть двухступенчатой.
Системы подготовки вентиляционного воздуха должны обеспечивать его чистоту в чистых помещениях в соответствии с таблицей 1 и поддерживать положительный перепад давления по отношению к окружающим помещениям более низкого класса чистоты.
Соседние помещения разных классов чистоты должны иметь перепад давления, как правило, 10 - 15 Па.
Внутренние и наружные поверхности фильтрокамер воздуховодов вентиляционных установок чистых помещений должны иметь покрытие, допускающее их обработку дезинфицирующим средством.
Необходимо регулярно проводить оценку эффективности работы фильтров с помощью приборов контроля запыленности воздуха и Дор-теста (испытание на герметичность и утечку). Замена или герметизация фильтрующего оборудования должны проводиться строго по показаниям приборов в соответствии с нормативными требованиями. Сроки замены должны определяться при увеличении сопротивления потоку воздуха вдвое по сравнению с исходной нормативной величиной, что свидетельствует о снижении производительности фильтра или о возможности его повреждения.
Производительность систем вытяжной вентиляции должна составлять 80 - 90 % от производительности систем приточной вентиляции для обеспечения требуемого подпора воздуха в чистых помещениях.
4.4.4 При производстве стерильных изделий медицинского назначения, контактирующих с кровью, целесообразно создание вертикальных ламинарных потоков, как во всем помещении, так и в отдельных зонах помещения для защиты наиболее ответственных участков или операций.
На чистом участке или в чистом помещении с вертикальным ламинарным потоком отверстия приточной вентиляции должны располагаться в потолке, а вытяжной - в полу или нижней части стен.
Чистые камеры (установки, создающие ламинарный поток стерильного воздуха, соответствующий классу чистоты С) должны отвечать следующим требованиям:
- направляющие поток панели, колпак и рабочие поверхности должны быть изготовлены из гладкого и прочного материала;
- фильтры предварительной очистки должны быть одноразовыми или из материала, позволяющего тщательно очищать их и использовать вновь;
- конечная фильтрация должна осуществляться через предварительно испытанные и герметичные фильтры тонкой очистки;
- скорость ламинарного потока должна быть в пределах 0,45 мк ± 20 %.
Работа установок ламинарного потока стерильного воздуха должна постоянно контролироваться согласно соответствующей инструкции и графику проверок.
4.4.5 При необходимости производственные помещения могут быть оборудованы системой кондиционирования приточного воздуха, которая должна:
- обеспечивать соответствующую степень очистки воздуха от механических частиц и микроорганизмов;
- автоматически регулировать климатические параметры (температуру и относительную влажность воздуха) для создания наиболее благоприятных условий для проведения технологического процесса и обслуживающего персонала;
- иметь высокую аэродинамическую устойчивость для поддержания оптимального распределения давления и других параметров воздуха в здании и его отдельных помещениях;
- исключать возникновение статического электричества и связанного с этим накопления пыли;
- характеризоваться малошумностью в работе;
- конструироваться с использованием материалов и антикоррозионных покрытий, стойких к дезинфицирующим средствам и пылеобразованию.
Отопление в производственных помещениях, должно быть воздушное, совмещенное с приточной вентиляцией. Установка местных нагревательных приборов в помещениях, где требуется чистота воздушной среды по классам А, В, С и D не допускается.
4.4.6 Каждое производственное здание должно быть обеспечено системой получения сжитого воздуха, а также технологической системой распределения его по всем помещениям, где он необходим.
Воздух, подаваемый от компрессоров без смазки, не должен иметь примесей и паров масла.
Для предотвращения конденсации пара в трубопроводах воздух должен быть обезвожен.
4.5 Освещение
4.5.1 Электроснабжение и электрическое освещение производственных зданий следует проектировать в соответствии со строительными нормами и правилами и другими действующими нормативными документами.
4.5.2 Все производственные, санитарно-бытовые и складские помещения должны быть обеспечены надлежащим освещением с интенсивностью света, достаточной для создания нормальных условий труда.
4.5.3 В чистых помещениях осветительные приборы должны быть встроены в углубления потолка, иметь пыленепроницаемую и пылезащищенную конструкцию и обеспечивать возможность легкой их замены.
4.5.4 На участках сварки, литья, нанесения печати и сборки изделий освещенность рабочего места рекомендуется не менее 500 лк, все остальные помещения могут иметь освещенность 300 лк.
На участках, требующих напряжения зрительного анализатора в связи с необходимостью точной координации движений и при малых размерах объектов различия (контроль деталей, готовых изделий, комплектация, сортировка и др.) должно предусматриваться комбинированное (общее и местное) освещение. Для местного освещения должны применяться светильники направленного света с учетом мероприятий по снижению отраженной блесткости.
4.6 Водоснабжение, канализация, сточные воды
4.6.1 Проектирование систем внутреннего водоснабжения, канализации и внутренних водостоков в производственных зданиях следует выполнять в соответствии со строительными нормами и правилами и другими действующими нормативными документами.
4.6.2 Целесообразно поступление водопроводной воды из автономной водопроводной сети под повышенным давлением.
В системе водоснабжения в трубопроводе при необходимости ставятся фильтры. В местах пересечения различных систем недопустим обратный сток жидкостей.
4.6.3 Трубопроводы систем водоснабжения должны:
- быть изготовлены из нержавеющей стали и рассчитаны на стерилизацию паром;
- иметь наклон вниз для полного отекания жидкости;
- не содержать участков, в которых может застаиваться вода (V-образные изгибы, «тупики», плохо сконструированные вентили).
4.6.4 Оборудование, применяемое для получения очищенной воды и воды для инъекций, должно монтироваться и эксплуатироваться таким образом, чтобы обеспечить получение необходимого количества воды требуемого качества. Условия получения, хранения и распространения воды должны препятствовать росту микроорганизмов (преимущественно с помощью постоянной циркуляции при температуре выше 80 °С).
4.6.5 Качество воды и подготовка оборудования для ее получения должно регулярно контролироваться в соответствии с инструкциями.
4.6.6 Система для стока жидких отходов производства должна быть приспособлена для предотвращения обратного тока жидкостей. Места их прохождения должны быть оборудованы соответствующей вентиляцией.
Системы для стока жидких отходов по возможности должны быть выведены из чистых помещений. При невозможности вывода таких систем они должны иметь эффективное приспособление с воздуходувом для очистки, предотвращающее возможный выброс через это приспособление, и устройство для дезинфекции.
4.6.7 По возможности следует создавать оборотные системы водоснабжения с обязательным осуществлением контроля за эффективностью очистки, а также за улавливанием и утилизацией шламов.
4.6.8 На охлаждение гидросистем оборудования и литьевых форм должна подаваться захоложенная оборотная вода.
4.7 Санитария
4.7.1 Производственные помещения следует содержать в соответствии с правилами санитарного режима в чистоте и надлежащем порядке. Не допускается разведение цветов, скопление мусора, появление насекомых-паразитов.
4.7.2 Каждое предприятие должно иметь подробную программу проведения санитарных мероприятий, устанавливающую:
- перечень помещений и оборудования, подлежащего уборке и обработке,
- методы и периодичность их проведения;
- перечень инвентаря, материалов, моющих и дезинфицирующих средств, применяемых при уборке помещений и обработке оборудования;
- перечень сотрудников, непосредственно выполняющих уборку помещений и обработку оборудования и руководящих их проведением.
Эти инструкции постоянно доводят до сведения соответствующего персонала и включают в программу подготовки и повышения квалификации.
4.7.3 Необходимо выделить помещение для хранения моющих и дезинфицирующих веществ, инвентаря и материалов, применяемых при уборке помещений и обработке оборудования.
4.7.4 Материалы и технические средства, используемые для чистки оборудования, должны проходить соответствующую профилактику.
4.7.5 Необходимо поочередное использование дезинфицирующих средств для предотвращения появлений устойчивых форм микроорганизмов.
Дезинфицирующие растворы должны быть стерильные. Во избежание роста микроорганизмов, разбавленные растворы необходимо хранить ограниченное время в заранее вымытых емкостях. Частично заполненные емкости нельзя доливать свежеприготовленными растворами.
4.7.6 Резервуары для растворов и растворителей, трубопроводы для подачи воды необходимо периодически чистить и содержать в образцовом порядке.
4.7.7 Нельзя использовать оборудование для чистки, которое стимулирует образование пыли, и трубопроводы для подачи воздуха с позитивным давлением. Пылесосы для чистки должны быть снабжены бактерицидными фильтрами.
4.7.8 Оборудование, используемое для чистки в чистых комнатах, не должно использоваться в других помещениях.
4.7.9 Следует регулярно проводить контроль содержания механических частиц и микроорганизмов в воздухе производственных помещений и контроль микробной контаминации оборудования по соответствующим инструкциям.
4.7.10 Работники, занятые в производстве медицинских изделий, должны соблюдать правила личной гигиены в соответствии с требованиями настоящего документа
5. Оборудование
5.1 Общие положения
5.1.1 Оборудование должно быть подобрано в соответствии с его назначением. Оборудование, используемое для производства и контроля качества медицинских изделий, должно размещаться так, чтобы максимально облегчить его подготовку к работе, эксплуатацию и обслуживание.
5.1.2 Вид, размер и характеристики оборудования и контрольно-измерительных приборов должны соответствовать проводимым технологическим процессам.
5.1.3 Контрольно-измерительные приборы и оборудование, используемые при изготовлении и контроле медицинских изделий, периодически должны подвергаться метрологической поверке и калибровке общепринятыми методами.
5.1.4 При производстве, упаковке, хранении, транспортировке и контроле качества медицинской продукции целесообразно использование сети компьютерной техники.
5.2 Конструкция оборудования
5.2.1 Оборудование должно соответствовать следующим требованиям:
- поверхности оборудования, соприкасающиеся с исходным сырьем, полупродуктами или готовым продуктом, должны быть гладкими и изготовленными из нетоксичного, стойкого к коррозии материала, который не реагирует с используемым сырьем или материалами и выдерживает обработку дезинфицирующими средствами и/или стерилизацию;
- все детали оборудования, контактирующие с используемыми сырьем, материалами и полупродуктами должны быть съемными для облегчения их мойки, обработки дезинфицирующими средствами или стерилизации;
- все передающие устройства (транспортеры, цепные передачи, приводы трансмиссии) должны быть закрыты или огорожены;
- должны быть исключены источники выделения в окружающую среду пыли, жидкости, смазочных масел;
- по возможности оборудование должно быть закрыто прозрачными колпаками для уменьшения вероятности попадания пыли и микроорганизмов на поверхность изготавливаемых изделий;
- конструкция оборудования должна обеспечивать возможность создания, при необходимости, ламинарных потоков в зоне технологической операции и удобство подключения к устройствам для отвода вредных веществ, выделяющихся в процессе изготовления изделий (желательно наличие встроенных в оборудование местных откосов);
- оборудование должно быть оснащено устройствами для предотвращения выделения конвекционного и лучистого тепла в помещение;
- оборудование должно иметь регистрирующие устройства для контроля параметров процесса, а также устройства сигнализации, извещающие о неисправности;
- люки и штуцера аппаратов должны быть оборудованы герметически закрывающимися крышками.
5.3 Размещение оборудования
5.3.1 Оборудование должно быть размещено таким образом, чтобы:
- оптимизировать потоки исходного сырья, материалов и свести к минимуму перемещение персонала;
- предотвратить возможность перекрестного загрязнения деталей, узлов и изделий в процессе их производства;
- предотвратить риск смешивания различных деталей, узлов, а также исключения одной из стадий производственного процесса;
- облегчить мойку, обработку, эксплуатацию и обслуживание оборудования.
5.3.2 Неисправное оборудование должно быть удалено из производственного помещения и помещений отдела контроля качества или, в крайнем случае, должно быть отделено и четко соответствующим образом промаркировано до его удаления из помещения.
5.4 Подготовка к работе и эксплуатация оборудования
5.4.1 Для каждого нового технологического процесса перед его внедрением в производство должна проводиться оценка монтажа и работоспособности оборудования, его валидация и аттестация; в случае замены или ремонта оборудования в соответствии с графиками должна проводится повторная валидация оборудования. Результаты ее проведения должны быть включены в отчет по валидации, а на каждую единицу оборудования должна быть помещена этикетка с указанием дат проведения последней валидации и повторной валидации.
5.4.2 Для проведения надлежащей эксплуатации следует регулярно проводить профилактические осмотры оборудования, a при необходимости - текущий ремонт.
5.4.3 Подготовку оборудования к работе следует проводить согласно инструкциям по его обработке дезинфицирующими средствами или стерилизации.
5.4.4 После обработки оборудования дезинфицирующими средствами или стерилизации необходимо проводить контроль качества подготовки оборудования к работе в соответствии с инструкциями.
Результаты контроля качества подготовки оборудования к работе, а также результаты проведения профилактических осмотров оборудования и текущего ремонта должны быть зафиксированы в специальном журнале.
5.4.5 Оборудование, используемое для изготовления деталей из сырья различных наименований и марок, должно очищаться таким образом, чтобы не допустить смешения различных видов и марок сырья.
5.4.6 Оборудование, используемое для работы в асептических условиях, по возможности, должно быть сконструировано и размещено таким образом, чтобы его ремонт можно было проводить за пределами чистых помещений, после завершения работ помещения следует обработать дезинфицирующими средствами.
5.4.7 На каждом предприятии должны действовать инструкции, устанавливающие:
- обязанности персонала по проведению обработки или стерилизации оборудования;
- график проведения обработки или стерилизации оборудования и производственных зон;
- график проведения профилактического осмотра и планового ремонта оборудования;
- порядок контроля стерильности или микробной контаминации оборудования после обработки или стерилизации, а также и процессе работы.
Записи полученных результатов следует вести в специальных журналах.
6. Процесс производства
6.1 Общие положения
6.1.1 Производство полимерных изделий, тканых и нетканых материалов медицинского назначения, контактирующих с кровью, имеет свою специфику, определяемую характером продукции и технологии. При этом используется соответствующее исходное сырье и вспомогательные, упаковочные и маркировочные материалы.
6.1.2 Неотъемлемой частью системы обеспечения качества производства продукции является составленная надлежащим образом документация. Она должна быть связана со всеми разделами «Правил...» и отражать их основные требования.
6.1.3 Процесс производства должен осуществляться в строгом соответствии с технологическим регламентом, отражающим требования «Правил...», что обеспечивает получение готовой продукции надлежащего качества.
6.2 Исходное сырье
6.2.1 Предприятие, выпускающее изделия медицинского назначения, контактирующие с кровью, должны иметь утвержденную в установленном порядке нормативную документацию на исходное сырье в виде стандартов предприятия.
6.2.2 На производстве должны быть утвержденные стандарты предприятия, которые включают в себя:
- описание сырья с указанием его названия, условного обозначения и/или кода;
- ссылку на имеющуюся нормативно-техническую документацию (НТД);
- указание возможных поставщиков сырья, с которыми согласована нормативная документация, объемы и сроки поставок;
- инструкция по отбору проб и проведению входного контроля с перечнем показателей, проверяемых при входном контроле;
- требования к качеству, включая дополнительные, с учетом специфики производства;
- надлежащие условия хранения и меры предосторожности при обращении с сырьем;
- срок годности или дату, после которой сырье не подлежит к использованию;
6.2.3 При получении партии сырья необходимо проверить совпадение сведения в бланке заказа, в накладной и в сертификате поставщика, отсутствие повреждения упаковки и ее чистоту, наличие документов, удостоверяющих качество сырья. Получение каждой партии и серии сырья должно регистрироваться в журнале.
6.2.4 Если одновременно было поставлено несколько различных партий одного наименования сырья, каждую партию и серию следует рассматривать отдельно в отношении отбора проб, проведения входного контроля по нормативной документации и выдачи разрешения на использование в производстве.
6.2.5 Полученное сырье и материалы следует подвергнуть входному контролю согласно действующей документации, для чего от каждой партии сырья и материалов отбирают средние пробы.
Отбор проб должен проводиться в специально оборудованных помещениях и с соблюдением условий, исключающих дополнительное загрязнение сырья и материалов. Желательно, чтобы отбор проб проводился одним уполномоченным сотрудником отдела контроля качества.
Любые отклонения от требований нормативной документации, в том числе, повреждения упаковки, которые могут повлиять на качество исходного сырья, должны быть зарегистрированы.
6.2.6 Полученное сырье должно быть снабжено этикеткой, содержащей следующую информацию:
- название продукции, условное обозначение и/или код;
- номер партии, серии;
- срок годности или дату, после которой сырье не подлежит к использованию;
При этом целесообразно использовать цветные этикетки. В процессе прохождения стадий контроля и в зависимости от его результатов (например, сырье разрешено к использованию, забраковано) этикетки заменяются.
6.2.7 Сырье и материалы должны храниться в помещениях для хранения, изолированных от основного производства. Для предотвращения смешения и перекрестного загрязнения необходимо предусмотреть отдельные помещения или участки приема, хранения и выдачи сырья и материалов.
При хранении должен быть обеспечен свободный доступ (свободный подход) к каждому виду сырья и материалов для его извлечения с места хранения.
6.2.8 Все материалы, предназначенные для потребительской и вторичной упаковки продукции должны поступать на предприятия от поставщиков в упакованном виде, обеспечивающем их сохранность и предотвращающем возможность вторичного загрязнения при хранении на протяжении всего срока годности.
Упаковочные материалы необходимо хранить в приспособленных для этого помещениях с учетом исключения возможности их загрязнения.
6.2.9 Перед растариванием транспортной тары (мешков с сырьем, ящиков и мешков со вспомогательными и упаковочными материалами) должна проводиться ее обеспыливающая обработка.
6.2.10 При проведении работ с сырьем и материалами должны строго соблюдаться существующие нормы санитарии, гигиены и техники безопасности.
6.2.11 Сырье и материалы должны выдаваться в производство при соответствии его требованиям НТД по разрешению отдела контроля качества. Выдача и баланс запаса сырья и материалов должны регистрироваться в журнале.
6.2.12 Сырье и материалы, проверенные отделом контроля качества и разрешенные им к использованию в производстве, должны храниться отдельно от тех партий, которые не прошли контроль или забракованы при контроле.
6.2.13 От каждой полученной партии сырья и материалов необходимо оставлять образцы в достаточном количестве на случай проведения повторных аналитических проверок.
6.2.14 При производстве изделий, предназначенных для контакта с кровью, особое внимание должно быть уделено условиям сохраняемости исходного сырья после приемки ОТК, а также во время доставки его к производственному участку и в процессе производства.
Все компоненты, входящие в состав стерильных лекарственных средств (например, компоненты для приготовления консервантов крови, инфузионных растворов и т.д.) должны регулярно подвергаться проверке на пирогенность и на стерильность или микробную контаминацию. Допустимое количество микроорганизмов должно быть указано в спецификациях на каждый вид сырья. При необходимости должно проводиться определение содержания механических примесей в исходном сырье.
6.2.15 Забракованные сырье и материалы должны быть направлены в специальную зону раздельного хранения материалов, должны быть промаркированы и возвращены поставщику или уничтожены, что должно быть документально оформлено.
6.2.16 За счет использования оптимальных процедур обработки и поддержания чистоты необходимо свести к минимуму потенциальную угрозу загрязнения окружающей среды технологического процесса за счет передачи материалов и изделий из зон временного хранения.
6.3 Технологический процесс производства. Контроль производства
6.3.1 Технологический процесс производства продукции должен осуществляться в соответствии с технологическими регламентами с целью обеспечения выпуска качественных изделий, соответствующих всем требованиям НТД.
6.3.2 Операции технологического процесса должны осуществляться и контролироваться квалифицированным персоналом с использованием необходимого оборудования в специально предназначенных для этих целей помещениях.
6.3.3 Нельзя допускать никакого отклонения от согласованной процедуры изготовления без предварительного согласования между руководителем производства и контролером по качеству и без предварительного введения получившего одобрение исправления или добавления в технологический регламент.
6.3.4 Все виды обработки и использования сырья, вспомогательных и упаковочных материалов и готовой продукции, включая приемку, карантин, отбор и анализ проб, хранение, маркировку, стерилизацию и упаковку, должны осуществляться в соответствии с письменными инструкциями и быть документально оформлены. Любые отклонения в ходе проведения производственных операций должны регистрироваться в журналах.
6.3.5 Необходимо разработать и придерживаться четкой системы, которая предусматривает, что перед началом производственного процесса необходимо освободить производственное помещение и все оборудование от всех исходных материалов, компонентов и изделий, которые не являются необходимыми для изделия, изготовление которого начинается.
6.3.6 В интервалах между переналадкой оборудования для серийного производства изделий необходимо практиковать чистку всей технологической линии, чтобы исключить вероятность загрязнения.
6.3.7 В процессе изготовления продукции необходимо промаркировать все приемные контейнеры или оборудование применительно к конкретному изделию, тщательно удалив ранее используемую на них маркировку.
6.3.8 Транспортирование сырья, вспомогательных и упаковочных материалов с цеховых складов должно осуществляться в соответствии со схемой организации технологического процесса изготовления изделий.
Раздача сырья к литьевому и экструзионному оборудованию должна осуществляться через технологический этаж к каждой машине вакуум-транспортом с возможностью переключения оборудования на другой вид сырья. Сушка сырья должна производиться в вакуум-сушильных шкафах. Желательна организация подсушки сырья в процессе транспортирования. Загрузка сыпучих продуктов при приготовлении растворов должна производиться по закрытым коммуникациям при использовании автоматических весов и дозаторов. Упаковочные и вспомогательные материалы, используемые в чистых помещениях, должны подаваться в эти помещения только в групповой и потребительской таре через грузовой шлюз.
6.3.9 В ходе технологического процесса должен быть обеспечен постоянный и периодический контроль за соблюдением параметров на стадиях и операциях технологического процесса в соответствии с технологическим регламентом и технологическими маршрутными и операционными картами: должны проводиться установленные документами контрольные испытания сырьевых, промежуточных и конечных продуктов.
6.3.10 Образцы для испытаний должны быть взяты контролером по качеству в соответствии с установленной процедурой. Если 100 % контроль должен выполняться производственным персоналом, то руководитель отдела контроля качества должен нести ответственность за утвержденный метод испытаний.
6.3.11 Внутрицеховая транспортировка деталей, узлов, изделий должна осуществляться в таре, исключающей возможность контаминирования изделий. Тара многоразового использования (контейнеры, биксы) должна быть изготовлена из материалов, устойчивых к воздействию дезинфицирующих веществ и должна быть идентифицирована в отношении находящегося в ней продукта. Перед нанесением новой надписи или метки все предшествующие записи должны быть удалены.
6.3.12 Особое внимание следует уделять процессам производства изделий однократного применения (стерильных) в асептических условиях, для подготовки которых необходимо выполнять комплекс мероприятий, описанных в соответствующих разделах (подготовка помещений, вентиляционного воздуха, оборудования, персонала к работе), кроме того, условия проведения технологического процесса должны обеспечивать:
- создание поточности технологического процесса;
- согласованность, безопасность и безаварийность работы всего технологического оборудования и оптимальную его нагрузку;
- исключение или сведение к минимуму контактов работающего персонала с исходным сырьем, деталями, узлами, стерильными растворами и готовыми изделиями в процессе обслуживания оборудования и при выполнении производственных операций;
- строгое документирование всех стадий технологического процесса, включая составление материального баланса;
- переработку образующихся отходов;
- автоматизацию и компьютеризацию технологических процессов, механизацию вспомогательных и погрузочно-разгрузочных работ.
6.3.13 Для раздува рукава при экструзии пленки и литья деталей в литьевые формы с пневмосбросом должен подаваться стерильный обеспыленный воздух.
Бобины с изготовленной пленкой и бухты трубки в случае, если указанные изделия используются в дальнейшем при проведении технологического процесса, упаковываются в полиэтиленовую пленку. Упаковка должна быть двойной; перед подачей в чистые помещения второй слой упаковки снимают.
6.3.14 При ручной сборке, упаковке в потребительскую тару, визуальном контроле внутрицеховая тара с комплектующими деталями, узлами, материалами, а также с собранными изделиями должна быть закрыта крышками или накрыта полиэтиленовой пленкой, которую допускается отгибать по мере опорожнения тары или при вкладывании собранных или проконтролированных изделий.
6.3.15 В ходе технологического процесса должны вестись соответствующие утвержденному регламенту записи технологических параметров процесса в операционных журналах, относящихся к каждой партии продукции. В журналах должны быть записи о забраковании, контроле качества и подписи установленных ответственных лиц.
6.3.16 Продолжительность хранения записей и образцов должна определяться отделом контроля качества.
6.3.17 При литье деталей изделий, предназначенных для контакта с кровью, использование консистентных смазок не допускается.
6.3.18 Нельзя допускать накапливания отходов в чистом помещении. Они должны собираться в соответствующую тару и регулярно и часто удаляться. Не допускается сбрасывание отходов на пол, пересыпание отходов в чистом помещении.
6.3.19 На участках проведения наиболее ответственных технологических операций (сборка, сварка, заполнение емкостей стерильными растворами) должно быть организовано воздухораспределение с однонаправленными ламинарными потоками с исключением застойных зон
6.3.20 В производстве мембран для тонкой очистки и стерилизующего фильтрования парентеральных растворов кровезаменителей формование пористой пленки должно проводиться с использованием изоляционной технологии. Нарезка фильтроэлементов и первичная упаковка мембран должна проводиться в ламинарном потоке очищенного воздуха.
6.3.21 Технология получения волокнистых фильтров для тонкой очистки и стерилизации воздуха должна исключать наличие незакрепленных волокон на рабочей поверхности фильтра.
6.4 Хранение
6.4.1 Промежуточные и готовые изделия, так же как и сырье, и материалы, должны храниться в отдельных помещениях (складах) в условиях, указанных в технологических регламентах и согласованных с отделом контроля качества.
6.4.2 Условия хранения должны быть таковы, чтобы предотвратить ухудшение качества, загрязнение или возможную порчу материалов и изделий.
6.4.3 Если на какой-то стадии хранения требуются специфические условия внешней среды, необходимо поддерживать и регулировать эти условия.
6.4.4 Условия хранения должны быть такими, чтобы облегчить ротацию материалов и изделий, дифференцирование их по партиям и обеспечить поддержание образцовой чистоты.
6.4.5 Доступ к материалам и изделиям в карантинной зоне должен быть ограничен и доступен только для лиц, имеющих на это специальное разрешение.
6.4.6 Изделия и материалы, которые забракованы или снова подготовлены к возврату после разбраковки, должны храниться в изолированной карантинной зоне для предотвращения смешивания их с другими изделиями и материалами.
Выдача и ротация их должны иметь разрешение контролера по качеству.
6.4.7 Для хранения вторичного сырья должно быть предусмотрено отдельное помещение в производственной зоне и в этом случае потенциальное загрязнение его должно быть сведено к минимуму.
6.5 Процесс этикетирования
6.5.1 Процесс этикетирования должен применяться, чтобы избежать путаницы при упаковке и ротации изделий со сходным внешним видом.
Необходимо также практиковать процедуры аттестации и идентификации технологических линий в интервалах между циклами.
6.5.2 Риск возникновения ошибок при упаковке и маркировке можно свести к минимуму путем:
- использования этикеток, наносимых валиком;
- выпуска известного (просчитанного) количества этикеток и строгого учета их использования;
- этикетирования партий на технологической линии, отличающихся одна от другой (заранее отпечатанные этикетки);
- использования электронных устройств кодирования и считывания кодов и электронных счетчиков этикеток;
- использования этикеток и прочих заранее отпечатанных материалов, которые предназначены для придания изделиям заметных отличительных признаков.
6.5.3 При завершении операции упаковки любые неиспользованные этикетки с кодом или упаковочные материалы должны быть уничтожены.
Некодированные материалы должны быть возвращены на склад согласно утвержденной процедуре с приложением документов.
6.5 Упаковка и маркировка
Упаковка должна быть такой, чтобы надежно содержать и защищать готовое изделие, а также для обеспечения сохранения изделия в стерильном виде.
Сохранение стерильности изделий должно быть также обеспечено правильным хранением и транспортированием.
Перед использованием любого вида упаковки следует проверить ее соответствие конкретным целям и назначению.
6.6.1 Упаковка.
Индивидуальная тара для стерильной продукции.
6.6.1.1 Стерильные изделия должны быть упакованы в герметичные единицы тары. В случае изделий, где требуется стерильность только внутренних поверхностей, требования к индивидуальной таре могут быть изменены и определены в нормативно-технической документации на конкретное изделие.
6.6.1.2 Целостность индивидуальной тары должна проверяться методом, изложенным в нормативно-технической документации.
6.6.1.3 Необходимо обеспечить надежную защиту стерильного изделия от загрязнения при хранении и транспортировании продукции до момента его непосредственного использования.
6.6.1.4 Индивидуальная тара для стерильной продукции должна быть такой, чтобы после ее первого вскрытия, нельзя было ее повторно закрыть (заварить) без отсутствия следов первоначального вскрытия.
6.6.1.5 Необходимо обеспечить условия, при которых изделие непосредственно перед использованием было бы в асептическом виде.
6.6.2 Контейнеры для групповой упаковки стерильной продукции.
6.6.2.1 Определенное количество стерильных изделий в индивидуальной таре может быть упаковано в контейнеры (ящики) для обеспечения защиты при хранении, манипулировании (переносе) и транспортировании изделий.
6.6.2.2 Дополнительная защита может быть обеспечена упаковкой контейнеров (ящиков) в контейнер для транспортирования.
6.7 Маркировка стерильной продукции
Единичный контейнер и контейнер для групповой упаковки должны иметь маркировку. Если невозможно или непрактично маркировать индивидуальную тару; как описано ниже, информация должна быть приведена на контейнере для групповой упаковки.
6.7.1 Индивидуальная тара.
На индивидуальной таре должно быть указано:
- описание содержимого или наименование продукции;
- слово «стерильный» рельефно, четко;
- слова «однократного применения» или «одноразового пользования», если необходимо;
- наименование производителя и поставщика;
- номер партии или дата изготовления, идентифицирующие партию и позволяющие проследить происхождение продукции;
- инструкция по применению, если необходимо;
- специальные меры предосторожности, если они имеются;
- срок годности (год/месяц) для изделий, которые имеют установленный срок годности.
6.7.2 На контейнерах для групповой упаковки должно быть указано:
- описание содержимого (наименование продукции), включая размер и количество содержимого, где это необходимо;
- слово «стерильный» рельефно, четко;
- наименование и адрес изготовителя или поставщика;
- номер партии или дата изготовления, идентифицирующие партию и позволяющие проследить ее изготовление;
- дата истечения срока годности для изделий, которые имеют установленный срок годности;
- инструкция по хранению, если она необходима.
6.7.3 Для нестерильной продукции на индивидуальной таре не следует указывать слово «стерильно», на контейнере групповой упаковки не следует указывать слово «стерильно» и «дату стерилизации».
6.7.4 Требования по маркировке представлены в приложении GMP.
6.8 Стерилизация изделий
6.8.1 Ответственным этапом технологического процесса изготовления продукции является стерилизация.
Стерилизация является процессом, который используется для инактивации жизнеспособных микроорганизмов на каком-то изделии в соответствии с желаемым пределом безопасности.
Процессы стерилизации должны тщательно контролироваться в соответствии с установленными регламентами нормами и должны обеспечивать воздействие параметров процесса во всем объеме продукции, при этом процесс стерилизации не должен ухудшать качество продукции.
6.8.2 Стерилизация изделий осуществляется методами газовой стерилизации окисью этилена (например, шприцев), радиационной стерилизации γ-облучением дозой или ускоренными электронами (например, устройств комплектных инфузионных и трансфузионных) и паровой стерилизации (например, контейнеров с консервантами).
Эффект стерилизации зависит от того, какого рода и какой сопротивляемости организмы находятся в стерилизуемом объекте. Чем меньше зараженность изделия микроорганизмами, тем выше вероятность стерильности продукции после стерилизации.
Независимо от природы и стойкости по отношению к процессу стерилизации, большая часть микроорганизмов находящихся на предназначенном для стерилизации изделий будет стерилизована в результате осуществления процесса стерилизации, и лишь очень незначительная их часть может оставаться на изделии.
С помощью принципов апробированной практики изготовления можно относительно легко и просто свести число находящихся на изделии микроорганизмов до минимума.
Выбранные процессы стерилизации должны проходить тщательную проверку, а их режимы регулироваться в жестких пределах.
Проверка достоверности должна осуществляться в соответствии с общей программой, которая обеспечивает гарантию стерилизации изделий выбранным методом.
6.8.3 Организация и проведение технологического процесса должны исключать возможность смешивания простерилизованной и еще не стерилизованной продукции. В этом случае следует использовать стерилизационное оборудование, вход и выход которого находятся в раздельных и несообщающихся помещениях.
Простерилизованная и непростерилизованная продукция должна быть четко разделена с помощью цветовых индикаторов или промаркирована.
6.8.4 При газовой стерилизации все оборудование участка газовой стерилизации должно быть выполнено во взрывобезопасном исполнении.
6.8.5 Внутренние поверхности стерилизатора, поверхности дверей со стороны камеры, загрузочные полки, транспортные тележки и другие приспособления для загрузки должны быть выполнены из материалов, стойких к коррозии и мало сорбирующих окись этилена.
6.8.6 Воздушные фильтры, установленные на линиях, подающих воздух в стерилизатор, должны обеспечивать задержку бактерий с минимальной эффективностью фильтрации 99,97 % для частиц размером 0,3 мкм.
Фильтры должны быть легко доступными для ежедневного техобслуживания.
6.8.7 В качестве обезвреживания отработанной после стерилизации газовой смеси или аварийного сброса рекомендуется метод сжигания в токе горячего газа или утилизация с помощью водного раствора.
6.8.8 Для проведения наиболее полной дегазации окиси этилена из изделий и уменьшения объема склада карантинного хранения необходимо перед отправкой продукции на склад карантинного хранения предусмотреть специальное помещение (кладовая дегазации), рассчитанное по объему, как минимум, на одну загрузку стерилизатора.
Кладовая дегазации должна быть оборудована приточно-вытяжной вентиляцией с кратностью воздухообмена не ниже 30 обменов/час.
6.8.9 Расчет рассеивания загрязняющих веществ и границ санитарно-защитной зоны необходимо производить по программам, рекомендуемым Госкомприродой СССР (в настоящее время Эфир-6, Версия-3).
6.8.10 Оформление технического проекта в части «Охрана окружающей среды» необходимо производить с учетом нормативных документов.
6.8.11 Участки радиационной стерилизации должны проектироваться в соответствии с «Унифицированными правилами устройства и безопасной эксплуатации радиационно-технических установок», М, 1988, «Основными санитарными правилами работы с радиоактивными веществами и другими источниками ионизирующих излучений. ОСТ 72/87», ГОСТ 20716 «Установки радиационные технологические. Термины и определения», ГОСТ 27632 «Ускорители заряженных частиц промышленного применения. Общие технические требования», а также в соответствии с научно-технической документацией, утвержденной Минздравом СССР.
6.9 Отходы
6.9.1 Складирование и транспортирование твердых и сыпучих промышленных отходов следует осуществлять по системе сметных контейнеров, исключающей ручную перегрузку отходов.
6.9.2 Невозвратные отходы производства должны помещаться в специальные контейнеры, имеющие соответствующую маркировку. Эти контейнеры следует выносить в специально отведенные места вне производственных помещений; их содержимое следует регулярно вывозить.
6.9.3 На предприятии должны быть предусмотрены специальные помещения для разборки и разбраковки узлов и изделий, не удовлетворяющих требованиям технологического процесса, а также помещения для переработки возвратных отходов.
6.9.4 Возвратные отходы собирают на всех стадиях производственного процесса по маркам и видам сырья в специальную тару, дробят и передают на предприятие по переработке пластмасс.
6.10 Контроль и регистрация производственных процессов
6.10.1 С целью предотвращения выпуска продукции, не соответствующей требованиям НТД, должен проводиться постадийный контроль процесса производства и осуществляться регистрационные записи, дающие информацию о каждом этапе изготовления и контроля каждой партии изделий.
6.10.2 Регистрационные записи должны выполняться одновременно с проведением процесса производства или контроля и включать:
- записи технологических режимов процесса при изготовлении деталей, узлов, полуфабрикатов, готовых изделий, осуществляемые работником в соответствующих журналах;
- записи обо всех проведенных операциях контроля и полученных результатах (выполняются в соответствующих журналах);
- акты о проведении приемо-сдаточных и периодических испытаний партий изделий на соответствие НТД;
- решение начальника отдела контроля качества о приемке или браковке партии изготовленных изделий.
6.10.3 Все регистрационные записи должны храниться в течение определенного периода времени, но не менее одного года после окончания срока годности изделия. Постадийный контроль процесса производства осуществляется сотрудниками цеховой лаборатории и отдела контроля качества в соответствии с действующими отраслевыми документами, технологическими инструкциями и операционными картами.
6.10.4 Периодичность проверок определяется руководством предприятия и отделом контроля качества применительно к данному изделию и процессу производства.
В ходе постадийного контроля проверяется:
- соответствие используемого сырья, вспомогательных и упаковочных материалов требованиям технической документации;
- санитарное состояние цехов и рабочих мест;
- выполнение регламентированных технологических операций и соблюдение технологических режимов работы.
При обнаружении отклонений от режима и норм технологического процесса должны быть выявлены причины и приняты меры по их ликвидации.
6.10.5 Отбор образцов для проведения операционного контроля и приемо-сдаточных испытаний должен проводиться сотрудниками отдела контроля качества (или в их присутствии) в соответствии с установленными инструкциями, утвержденными техпроцессами, техническими условиями в количестве, достаточном для проведения необходимых анализов ОКК предприятия-изготовителя и органами государственного контроля во время хранения;
- образцы исходного сырья, деталей узлов, готовых продуктов, НТД, методики проведения анализов, записи, относящиеся к изделиям;
- документацию на все изготовленные партии, копии результатов анализов исходного сырья, полупродуктов и готовых изделий.
Образцы исходного сырья, материалов и готовых изделий, а также эталонные образцы деталей, должны храниться при условиях, определенных предприятием-изготовителем.
6.11 Контроль готовой продукции
6.11.1 Готовая продукция должна быть проверена на соответствие действующей нормативно-технической документации отделом контроля качества. Образцы продукции, отобранные для контроля качества должны адекватно отражать партию продукции.
6.11.2 Для проведения испытаний должны быть составлены и утверждены методики в письменной форме. Образцы готовой продукции должны проходить приемо-сдаточные и периодические испытания, установленные НТД. Результаты испытаний должны быть документированы, журналы должны храниться в течение срока годности продукции.
6.11.3 От каждой партии продукции в специально отведенном помещении, в условиях, оговоренных НТД, должны храниться арбитражные образцы готовой продукции в потребительской таре в течение 3 - 5 лет.
Сведения о хранении арбитражных образцов должны быть также документированы в арбитражном журнале.
Ответственность за хранение арбитражных образцов должна быть возложена на отдел контроля качества.
6.11.4 Отдел контроля качества должен быть не зависим от производства и продажи продукции, должен иметь прямой выход на руководителя предприятия.
Отдел контроля качества должен иметь право останавливать производство в случае забракования продукции на любой стадии технологического процесса и иметь право прекращать отгрузку продукции на реализацию, при выявлении брака в технологическом процессе.
При обнаружении брака должны быть выявлены причины его возникновения и приняты меры по их ликвидации.
6.11.5 Каждая партия конкретного вида радиационно стерилизуемой продукции должна пройти контроль на инициальную контаминацию, характеризующуюся средним числом микроорганизмов, обсеменяющих единицу продукции.
Для каждого вида продукции устанавливаются предельно допустимые показатели инициальной контаминации.
Контаминированность продукции до стерилизации зависит от технологии процесса и санитарно-гигиенических условий на производстве. Поэтому должно доводиться также определение радиационной устойчивости (радиорезистентности) микроорганизмов, выделенных из микрофлоры цехов сборки и упаковки и из микрофлоры готовой продукции («Микробиологический мониторинг производственной среды» МУК 4.2.734-99 Департамент ГосСЭС МЗ РФ, 1999 г.).
Порядок отбора проб продукции и определение инициальной контаминации должны проводиться в соответствии с «Методикой оценки санитарно-гигиенического состояния на предприятиях, выпускающих радиционно-стерилизуемую продукцию медицинского назначения» № 2534-82 от 11.02.1982 г.
6.11.6 Радиационно-стерилизованные медицинские изделия должны пройти контроль стерильности в соответствии с приказом Минздрава СССР и Минмедпрома № 376/207 от 19.04.1974 г. (О введении в действие «Свода правил, регламентирующих проведение радиационной стерилизации медицинской продукции») и приказа Минздрава СССР № 60 от 17.01.1979 г. (О мерах по дальнейшему укреплению и развитию дезинфекционного дела).
6.11.7 Контроль стерильности медицинских изделий, стерилизованных радиационным способом должен проводиться в соответствии с «Методическими указаниями по контролю стерильности медицинских изделий, стерилизованных радиационным способом», утвержденными приказом Минздрава СССР и Минмедпрома № 964/410 от 17.09.1979 г. «О порядке проведения контроля стерильности радиационно-стерилизованных изделий на предприятиях Минмедпрома».
6.11.8 Все изделия из полимерных материалов одноразового использования должны проходить после стерилизации (вне зависимости от способа стерилизации) биологический контроль, включающий испытание на стерильность, пирогенность, токсичность и санитарно-химический контроль.
Служба биологического контроля должна включать в себя бактериологическую и токсикологическую лаборатории, лабораторию испытания на пирогенность.
Контроль готовой продукции по указанным показателям должен проводиться аккредитованными лабораториями.
6.11.9 Шприцы инъекционные однократного применения, стерилизованные газовым и радиационным методом, должны подвергаться санитарно-химическим, токсикологическим и биологическим испытаниям (стерильность и пирогенность) в соответствии с «Регламентом, устанавливающим порядок проведения санитарно-химических, токсикологических и биологических испытаний стерилизованных шприцев инъекционных однократного применения» (1991 г.) Минздрава СССР, НПО «Экран», ВНИИИМТ.
Контейнеры для крови и ее компонентов должны подвергаться испытаниям санитарно-химическим, токсикологическим и биологическим в соответствии с ГОСТ Р 50855-96.
Устройства комплектные эксфузионные, трансфузионные и инфузионные, магистрали и трубки к аппаратам искусственного кровообращения, сосудистые катетеры, протезы кровеносных сосудов, мембраны и фильтры для крови и ее препаратов, кровезаменителей должны подвергаться испытаниям в соответствии с ОСТ 42-513-99 «Устройства комплектные эксфузионные, инфузионные и трансфузионные однократного применения. Требования химической и биологической безопасности. Методы испытаний в условиях предприятий-изготовителей».
- стерильность по указанным в п. 6.11.7 методическим рекомендациям... (приложение к приказу № 60 Минздрава СССР от 17.01.1979 г.)
- пирогенность - по «Методике контроля пирогенности медицинских изделий однократного применения, стерилизованных радиационным и газовым методом», ВНИИИМТ 26.10.1992 г.
- токсичность по «Методике контроля токсичности медицинских изделий однократного применения, стерилизованных радиационным или газовым методом», Минздрава СССР от 01.03.1991 г.
Оценки биологического действия медицинских изделий целесообразно проводить в соответствии с ГОСТами Р ИСО 10993.
6.11.10 При положительных результатах испытаний на стерильность стерилизованная продукция считается пригодной для реализации при условии соответствия физико-механическим и техническим требованиям НТД.
Комплектующая продукция, например, иглы, поступившая с других предприятий, также должна пройти контроль стерильности.
6.12 Контроль производственной и окружающей среды
6.12.1 На предприятиях должен быть организован плановый санитарный контроль за состоянием воздуха рабочей зоны, атмосферного воздуха промышленных площадок и примыкающих жилых застроек, а также сточных вод. Контроль должен осуществляться бактериологической лабораторией, а прочие замеры должны производить другие службы: лаборатория охраны окружающей среды, лаборатория физико-химических исследований при контроле и методическом руководстве санитарной службы.
6.12.2 При контроле воздушной среды производственных помещений и атмосферы, точки отбора проб согласуются с Государственной санитарной службой на местах. Одновременно устанавливается периодичность контроля воздушной среды, которая будет зависеть в каждом конкретном случае от класса опасности, летучести и количества вредных веществ, представленных в таблице 4.
6.12.3 При контроле воздушной среды в производстве и атмосфере необходимо ориентироваться на наиболее токсичные компоненты газовыделений и вредные вещества.
6.12.4 Контроль воздушной среды на содержание вредных веществ должен проводиться с учетом основных стадий технологического процесса, размещения источников выделения вредных веществ и их распространения по производственным помещениям в связи с особенностями циркуляции воздуха.
6.12.5 На обследуемом рабочем месте и на каждой стадии технологического процесса или отдельной операции должно быть последовательно отобрано такое количество проб (но не менее пяти), которое было бы достаточным для достоверной характеристики состояния воздушной среды данной точки и оцениваемой стадии производства.
6.12.6 При возможности поступления в воздух рабочей зоны веществ 2-го класса опасности, которые могут вызывать тяжелые острые отравления, необходимо проводить преимущественно непрерывный контроль.
При поступлении в воздух рабочей зоны остальных вредных веществ 2-го класса опасности санитарный контроль необходимо проводить не реже 1-го раза в месяц.
При поступлении в воздух рабочей зоны вредных веществ 3-го и 4-го классов опасности санитарный контроль должен осуществляться:
- не реже одного раза в месяц, если на загрязнении воздуха рабочей зоны оказывают влияние недостаточная стабильность режима технологического регламента, микроклиматические условия, изменение технического состояния оборудования, вентиляции и пр.;
- не реже 1 раза в квартал - в остальных случаях.
Таблица 4
Перечень вредных веществ, выделяющихся в производстве изделий медицинского назначения из полимерных материалов.
|
Вредные вещества, подлежащие определению |
ПДК мг/м3 |
Класс опасности |
Методические указания на методы определения |
|
|
Литье, экструзия, сварка, прессование, механическая обработка: Полилефины: Полиэтилен |
формальдегид |
0,5 |
2 |
в. XX, МУ № 3123. М., 1984, с. 143 |
|
ацетальдегид |
5 |
3 |
в. VI - VII, МУ № 2563. М., 1982, с. 7 |
|
|
углерода оксид |
20 |
3 |
в. XIX, МУ № 2905-83, М., 1984, с. 113 |
|
|
уксусная кислота |
5 |
3 |
в. XIX, МУ № 2895-83, М., 1984, с. 72 |
|
|
непредельные углеводороды (этилен, пропилен) |
100 |
4 |
в. XIX, МУ № 2818-83, М., 1984, с. 171 |
|
|
этилена оксид |
1 |
2 |
в. I - V ТУ № 122-1/11, М., 1972. с. 103 МУ № 1682-77, с. 150 |
|
|
Полипропилен |
формальдегид |
0,5 |
2 |
См. выше |
|
пропионовая кислота |
20 |
4 |
в. XIX МУ № 2895-83, М., 1984, с. 72 |
|
|
углерода оксид |
20 |
3 |
См. выше |
|
|
непредельные углеводороды (этилен, пропилен) |
100 |
4 |
См. выше |
|
|
Газовая стерилизация |
этилена оксид |
1 |
2 |
См. выше |
|
Изготовление игольных заготовок: СОЖ водоэмульсионные |
масляная аэрозоль |
5 |
3 |
в. ХIX МУ № 2896-83, М., 1984 |
|
окись углерода |
20 |
3 |
См. выше |
|
|
ангидрид сернистый |
10 |
3 |
в. I - V МУ 1642-77, М., 1981 |
|
|
масляная аэрозоль |
5 |
3 |
См. выше |
|
|
СОЖ масляные |
углеводороды предельные |
300 |
4 |
в. ХIX МУ № 2892-83, М., 1984 |
|
углеводороды непредельные |
100 |
4 |
См. выше |
|
|
углерода оксид |
20 |
3 |
См. выше |
|
|
Обезжиривание игл |
тетрахлорэтилен (перхлорэтилен) |
10 |
3 |
в. VIII, МУ № 2769-33, М., 1983 |
|
фосген |
0,5 |
2 |
в. I - V, ТУ № 583-65, М., 1972 в. I - V МУ № 1677-77, с. 183 |
|
|
Отжиг игольных трубок |
аммиак |
20 |
4 |
в. I - V ТУ № 122-1/199, М., 1972 в. I - V, МУ № 1637-77, с. 58 |
6.13 Контроль чистых производственных помещений
Чистые производственные помещения должны быть валидированы на соответствие настоящим Правилам.
6.13.1 Каждое предприятие должно иметь подробную программу проведения санитарных мероприятий, устанавливающую:
- перечень помещений, подлежащих уборке;
- список оборудования, подлежащего обработке;
- периодичность уборки помещений и обработки оборудования;
- методы уборки помещений и обработки оборудования;
- инвентарь, материалы, моющие и дезинфицирующие средства, применяемые при уборке помещений и обработке оборудования;
- перечень сотрудников, непосредственно выполняющих уборку помещений и обработку оборудования,
- перечень сотрудников, на которых возложено руководство проведением уборки и обработки.
Эти инструкции должны быть включены в программу подготовки, инструктажа и повышения квалификации персонала.
6.13.2 Необходимо выделить помещение для хранения моющих и дезинфицирующих веществ, инвентаря и материалов, применяемых при уборке оборудования.
6.13.3 Необходимо поочередное использование дезинфицирующих средств для предотвращения появления устойчивых форм микроорганизмов. Дезинфицирующие растворы должны быть стерильны. Во избежание роста микроорганизмов, разбавленные растворы следует хранить ограниченное время в заранее продезинфицированных, плотно закрытых емкостях. Частично заполненные емкости нельзя доливать свежеприготовленными растворами.
6.13.4 Следует регулярно проводить контроль содержания механических частиц и микроорганизмов в воздухе производственных помещений и контроль микробной контаминации оборудования, поверхностей помещения, спецодежды и рук персонала.
6.13.5 В случае повышения запыленности воздушной среды, следует провести ежесменную влажную уборку помещения, а повторный контроль запыленности воздуха производить не ранее, чем через один час после уборки.
6.13.6 В случае превышения количества непатогенных микроорганизмов в воздушной среде свыше допустимого, а также в случае обнаружения споровых микроорганизмов, следует срочно провести обработку 6 % раствором перекиси водорода и затем провести повторный контроль.
6.13.7 В случае обнаружения микробных тел в воздухе на выходе из приточных вентиляционных систем, следует заменить фильтр тонкой очистки и выполнить влажную уборку данной приточной камеры.
6.13.8 В функции баклаборатории должно быть включено:
- анализы по содержанию микроорганизмов в воздухе производственных помещений и микробной обсемененности поверхностей оборудования, помещений, спецодежды, рук персонала;
- анализы по микробной обсемененности продукции (контаминации);
- проверке продукции на стерильность.
Количество и периодичность проведения анализов приведены в таблице 5.
Таблица 5
Микробиологический контроль
|
Периодичность контроля |
Количество образцов на анализ, шт. |
|
|
1. Контроль микробной обсемененности продукции |
Каждая партия |
При количестве изделий в партии до 1000 - 3 ÷ 6 изд. От 1000 до 5000 - 6 ÷ 10 изд. Свыше 10000 - 14 ÷ 20 изд. |
|
2. Контроль стерильности продукции |
Каждая партия или согласно приказу № 964/410 от 17.09.1979 г. |
Согласно методике контроля стерильности ГОСТ 25047-87. |
|
3. Контроль обсемененности поверхности помещений и оборудования |
1 раз в неделю. После достижения стабильного санитарного состояния производства 1 раз в месяц. |
5 проб с поверхности. |
|
4. Контроль обсемененности воздуха |
1 раз в неделю. После достижения стабильного санитарного состояния производства 1 раз в месяц. |
От 1 до 5 проб в зависимости от площади помещения. |
|
5. Контроль обсемененности спецодежды |
То же |
От 2 до 5 проб с объекта у 10 - 30 % занятого персонала. |
|
6. Контроль обсемененности рук персонала |
- » - |
У 10 - 30 % занятого персонала. |
Примечание: 1. Партией считается количество продукции, простерилизованной в течение суток, или за один технологический цикл, или в одном автоклаве.
2. Заключение о стерильности партии может быть получено не ранее, чем через 8 суток после проведения анализа.
7. Документация
7.1 Большое внимание должно быть уделено подготовке документации, существенно влияющей на обеспечение качества.
Такая документация, как минимум, должна включать следующие материалы:
- руководство по обеспечению качества;
- процедуры (документы, методики и др.) программы обеспечения качества;
- проектная документация;
- закупочная документация;
- производственная документация;
- процедуры специальных технологических процессов;
- документация о проверках (контроле, аудите).
7.2 В руководство по обеспечению качества, как минимум, должны быть включены следующие вопросы:
- применение программы (определение организационной структуры);
- обязанности администрации и организация работ (политика и организация управления, рассмотрение администрацией программы обеспечения качества, полномочия и обязанности представителя администрации по решению вопросов качества, полномочия организационных структур, проведение контроля работы, обучение и тренировка персонала);
- процедуры (документы) программы обеспечения качества;
- контроль выполнения руководством (положение по рассмотрению, корректировке и контролю руководством).
Процедуры программы обеспечения качества должны охватывать следующие элементы программы:
- заявка на подряд и контракт;
- проектирование;
- документация;
- измерительное и испытательное оборудование;
- закупки;
- план(ы) контроля и испытаний;
- входной контроль;
- контроль в процессе производства;
- состояние технического контроля;
- идентификация и прослеживаемость;
- производство;
- упаковка и отгрузка;
- регистрация данных о качестве;
- обращение и хранение;
- корректирующие действия;
- проверки (аудит) качества.
В каждой процедуре программы следует документировать цель и сферу действия процедуры, кто и за что отвечает, как, когда и где выполняется каждый этап, какие материалы, оборудование и документация используются, как контролируется выполнение.
7.3 Документация должна быть тщательно и подробно разработана, подписана ответственными лицами и утверждена руководством с указанием даты.
Внимание к деталям существенно при подготовке документов и инструкций, в особенности для того, чтобы исключить двойное толкование. Документы и инструкции должны быть понятны всем, кто будет их выполнять. Копии документов должны быть четкими, разборчивыми и нестираемыми.
Документация должна быть выполнена печатным способом (на машинке или на компьютере, или фотографированием).
Правильность записей должна контролироваться ответственными лицами.
В случае внесения изменений, могут допускаться исправления от руки. В этом случае, внесенные исправления должны быть завизированы ответственными правомочными лицами.
При пересмотре и замене документации, замененные первые экземпляры и их копии должны быть уничтожены. Если замененные первые экземпляры должны храниться, то они должны быть ясно помечены и сохраняться таким образом, чтобы была исключена путаница в текущих документах.
Все изменения и замена документов должны быть запротоколированы. Внесение изменений и замена документов должны проходить тот же уровень согласования и утверждения, что и первичные документы. Вся устаревшая документация должна быть изъята со всех мест ее применения.
Доступ к подлинникам документов должны иметь уполномоченные, ответственные лица.
Записи информации в компьютере должны быть защищены кодом, а также продублированы записями на дискетах, микрофильмах и бумаге.
Вся система разработки, оформления, согласования, утверждения, размножения и распределения документации должна периодически контролироваться.
Все копии документов и инструкций должны находиться, по возможности, вблизи рабочего места и операции, которая должна выполняться в соответствии с инструкцией.
Вся существенная документация, влияющая на качество, должна быть рассмотрена перед началом выпуска продукции.
7.4 Основными базовыми документами, по которым проводят процесс изготовления продукции на предприятии, является технологический регламент производства (пусковой, опытный, опытно-промышленный) и технические условия на изделие. Дополняют его и участвуют в технологическом процессе изготовления продукции, разработанные на основе технологического регламента - стандарты предприятия, инструкции, рабочие журналы записей параметров входного, операционного контроля, контроля проведения испытаний, методики контроля, маршрутные и операционные карты, документ о качестве, паспорт и другая сопроводительная документация.
7.5 Технические условия и стандарты предприятия на сырьевые материалы, рабочие журналы на входной контроль поступающего в производство сырья должны включать:
- описание материала и компонента (детали) и рисунки, если это необходимо;
- название материала и его кодовый номер;
- указание на поставщика (изготовителя) материала;
- описание метода упаковки;
- все инструкции по технике безопасности для ручной обработки и применения;
- инструкции по порядку отбора проб;
- методы испытаний по контролю качества, которые должны быть выполнены (включая аналитические методы), классификацию дефектов и пределы приемлемости;
- требования для стандартных образцов (стандартные образцы и отбор образцов должны быть согласованы поставщиком);
- условия хранения;
- периодичность повторных испытаний хранящегося материала, когда это необходимо.
7.6 Технологические документы по описанию производства (маршрутные и операционные карты, технологические и другие инструкции) должны включать:
- описание оборудования и материалов, которые должны использоваться;
-подробные сведения обо всех мерах предосторожности, которые следует предпринять;
- постадийные инструкции по изготовлению;
- подробности проверки правильности протекания процесса, которая должна проводиться производственным персоналом;
- инструкции по процедурам, связанным с качеством продукции;
- инструкции по контролю принятых и забракованных промежуточных и конечных продуктов, в том числе, передача в зону стерилизации, склады или на уничтожение.
Стандарты предприятия, описания и инструкции на промежуточные и конечные детали и продукцию должны содержать:
- название продукта и его кодовый номер;
- описание, включая в необходимых случаях фотографии и/или рисунки физической формы продукта, вместе со стандартными (эталонными) образцами;
- инструкции по отбору, периодичности и методу испытаний;
- классификацию средств и пределы приемлемости.
7.7 Записи в технологических журналах по изготовлению партий продукции должны содержать:
- запись этапа изготовления партии на основе технологического регламента;
- обозначение производственной линии (места), на которой производилось изделие и дата записи;
- обозначение номера партии;
- количество сырьевых материалов, компонентов и промежуточных продуктов и номер соответствующей партии;
- количество произведенного продукта с указанием номера (кода) партии, если необходимо, количество сырьевых контейнеров или контейнеров с готовым продуктом;
- результаты всех контрольных операций и фамилии лиц, отбиравших образцы;
- подробности любого отклонения от регламента процесса (если даны разрешения на отклонения, то необходимо указание фамилии ответственного лица);
- записи о проведении стерилизации.
7.8 Записи в технологических журналах о забраковании и аннулировании продукции должны содержать:
- записи о браковке или рекомендательной процедуре, утвержденной контролером по качеству и лицом, которое назначено инициировать или координировать процедуру;
- методы, используемые для эффективной отбраковки или для предотвращения выпуска партии(й);
- методы извещения и предупреждения;
- описание продукта, его кодовый номер;
- номер партии;
- действия, которые следует предпринять (продолжение отбраковки, количество продукта, указания для отправки в карантин);
- причина действий и рекомендации по действиям в опасных условиях.
7.9 К документам, охватывающим другие аспекты оптимальной организации труда (производства) относятся также журналы записей по процедурам:
- чистка и уход за зданием и оборудованием;
- поверка оборудования;
- контроль окружающей производственной среды;
- обучение персонала, особенно в отношении необходимой производственной дисциплины и гигиены;
- возвращение неиспользованных материалов на склад;
- инструкции по материалам и продуктам, не отвечающим техническим условиям;
- обращение с возвращенной продукцией.
8. Валидация
8.1 Валидация является одним из важнейших и ответственных этапов работы предприятия в обеспечении качества производимой продукции по GMP и требует значительных усилий большого количества персонала для ее выполнения.
Валидация заключается в последовательной тщательной проверке всего производственного процесса производства продукции и всех факторов, могущих повлиять на ее качество (условий производства, оборудования, приборов, проектной документации и т.д.), в документальном оформлении результатов проверки и подтверждении того, что проверенный производственный процесс соответствует предъявляемым к нему требованиям нормативно-технической, конструкторской и технологической документации, является воспроизводимым и повторяемым, а конечная продукция производства отвечает всем требованиям, предъявляемым к ней.
8.2 Для организации работ по проведению валидации должен быть создан коллектив (отдел валидации, валидационные комиссии) высококвалифицированных специалистов по направлениям валидационной работы.
Основные направления деятельности коллектива (отдела) следующие:
- Валидация и согласование проектной документации на строительство производственных участков или реконструкцию действующего производства в соответствии с требованиями методических указании «Производство лекарственных средств. Валидация. Основные положения»;
- квалификация установленного основного технологического оборудования и проверка коммуникаций и контрольно-измерительных приборов;
- квалификация подготовки к работе и эксплуатации основного технологического оборудования и контрольно-измерительных приборов;
- валидация производственных чистых помещений и текущий контроль;
- валидация этапов технологического процесса производства, в том числе, валидация процесса стерилизации;
- контроль изменений.
8.3 Основные положения валидации и аттестации должны быть сформулированы в валидационном мастер-плане или в руководстве по качеству.
Валидационный мастер-план должен определять объем и описание работ по валидации, перечень объектов валидации, план-график работ с указанием сроков проведения этапов, денежных затрат и ответственных специалистов за проведение работ.
Валидационный мастер-план должен быть кратким, не должен повторять информацию, содержащуюся в других документах и должен содержать ссылки на действующие документы, правила и инструкции, описания, протоколы и отчеты.
В валидационном плане работ должны быть акцентированы критические технологические операции и оборудование, критические изменения в сырьевых материалах и соответствующий контроль процесса и продукции с целью проведения валидационного исследования и условиях «наихудшего случая».
8.4 В подготовительный период перед валидацией должны быть подготовлены и переоформлены все необходимые документы в соответствии с требованиями GMP и настоящих «Правил ...»:
- маршрутные и операционные карты технологических процессов производства;
- инструкции по подготовке к работе и эксплуатации оборудования;
- инструкции по подготовке и очистке помещении;
- инструкции по контролю чистых помещений;
- инструкции по гигиене персонала;
- инструкции по обслуживанию технического оборудования;
- инструкции по организации метрологического обеспечения;
- инструкции по ведению отдельных этапов и операций технологического процесса;
- инструкции по ведению и контролю процесса стерилизации;
- инструкции по контролю готовой продукции;
- инструкции по хранению и отгрузке продукции и др.
Должен быть определен порядок хранения и распространения документов, внесения изменений и уничтожения устаревших документов.
8.5 При проведении первичной валидации следует уделить внимание подготовке оборудования, коммуникаций, комплектации необходимыми контрольными и измерительными приборами, получению сертификатов соответствия на оборудование.
В процессе аттестации установленного и функционирующего оборудования должны быть выявлены недостатки в работе оборудования, отклонения от допустимых пределов.
Следует уделить внимание валидации и аттестации чистых производственных помещений на соответствие зонам А, С и D для производства изделий медицинского назначения из полимеров, тканых и нетканых материалов.
8.6 В процессе валидации следует провести оценку каждого этапа технологического процесса производства продукции, основываясь на опыте обученных квалифицированных специалистов, провести испытания в критических ситуациях, чтобы проверить процесс и убедиться в его возможностях обеспечить выпуск качественной готовой продукции в соответствии с требованиями НТД.
Первичная валидация должна быть проведена до начала выпуска серийной продукции и поставке ее потребителю.
Процесс валидации должен быть всесторонне документирован. Должен быть составлен отчет и протоколы о проведенном процессе валидации с учетом условий «наихудшего случая» и данными о неудачных результатах, проведено сравнение полученных результатов с ожидаемыми.
В заключение должна быть проведена завершающая официальная приемка работы уполномоченными ответственными. Документация по валидации должна быть утверждена руководством предприятия.
8.7 Процесс валидации производства не должен быть разовым, преддверием начала серийного производства. Он должен периодически повторяться для подтверждения надежности производства.
Повторная валидация (ревалидация) должна проводиться в тех случаях, если проводят:
- изменения в технологический процесс и соответствующие корректировки в технологический регламент;
- изменения в маршрутные и операционные карты, инструкции, методики контроля;
- изменения в конструкторскую документацию на изделия и в технологическую оснастку на их изготовление;
- изменения конструктивные в оборудование или замена оборудования, или установка нового оборудования;
- изменения при закупке сырья, смена поставщика, замена марки сырья;
- изменения при замене упаковки и маркировки продукции, этикетирования ее;
- ремонт производственных помещений, переоборудования их, переоборудования систем вентиляции, систем подачи сырья;
- выявления сбоев по инициальной контаминации и стерильности продукции.
Повторная периодическая валидация должна регулярно проводиться также в соответствии с плановым графиком валидаций производства.
Возможно, при хорошо отлаженном технологическом процессе, проведение ретроспективной валидации (при необходимости) по имеющейся на предприятии необходимой документации (рабочих журналов контроля процесса, результатов входного контроля сырья, результатов проверки средних сроков сохраняемости изделий при арбитражном хранении и др.).
Важным элементом процесса обеспечения качества является контроль внесения изменений на этапах ведения производственного процесса.
Все изменения должны быть документированы, должна быть проведена тщательная оценка влияния изменения на качество готового изделия, оценен объем ревалидации. Все вносимые изменения должны быть согласованы, приняты заинтересованными службами предприятия и утверждены в установленном порядке. Конечное изделие должно быть проверено на соответствие нормативно-технической документации.
Валидирование процесса производства должен быть закончен отчетом ответственных лиц (лица) с заключением о соответствии процесса требованиям нормативно-технической, технологической документации.
9. Сбор информации о качестве продукции в процессе ее эксплуатации. Рекламации и отзыв продукции с рынка
9.1 Качество продукции есть степень соответствия данного продукта (изделия) требованиям, предъявляемым к нему потребителем. Поэтому сбор информации о поведении изделия в процессе его эксплуатации является чрезвычайно важным делом.
С этой целью на предприятии должна быть создана специальная служба (обслуживания) потребителя-покупателя или определен сотрудник, ответственный за сбор информации о качестве продукции, об эксплуатационных характеристиках изделий.
В обязанности службы обслуживания должно быть включено:
- инструктаж потребителя и указания по использованию изделий;
- оказание услуг и обслуживание, организация правильной эксплуатации и замена не удовлетворяющей потребителя продукции;
- сбор и анализ рекламаций, и принятие необходимых мер.
9.2 Первый и самый распространенный метод получения информации о поведении изделий в процессе эксплуатации состоит в сборе и анализе рекламаций от потребителя.
Служба обслуживания должна исследовать, оценивать и хранить письменные и устные претензии относительно подлинности, качества, прочности, безопасности, эффективности или рабочих характеристик изделий.
Рассмотрение рекламаций должно проводиться тщательно, во внимание должны приниматься все жалобы от всех потребителей, независимо от их влияния на сбыт продукции в данный момент, необходимо обращать внимание не только на количество, но и характер рекламаций.
9.3 Каждая полученная рекламация должна быть документально зафиксирована на бланке для регистрации жалоб потребителей.
В документе должны быть вписаны следующие данные:
- наименование изделий;
- обозначение нормативно-технического документа (технических условий);
- номер партии;
- дата изготовления;
- срок годности;
- отметка о стерилизации;
- дата получения жалобы;
- наименование или фамилия потребителя;
- адрес потребителя;
- изложение и детали жалобы;
- перечень приложений (письмо с жалобой, образец или фотография дефектного изделия);
- подпись лица составителя.
9.4 Бланк регистрации жалобы должен быть передан в отдел контроля качества, который должен провести соответствующее расследование, установить причину(ы) возникновения дефекта. Если расследование не проводится, подразделение должно хранить документ, в котором указывается причина возникновения дефекта и фамилия лица, ответственного за принятие решения не проводить расследования, дата принятия решения.
Любая претензия потребителя, включая возможную неспособность изделия удовлетворить какое-либо из его требований, должна быть рассмотрена, оценена и расследована. Любую претензию, относящуюся к причинению травмы, смерти или любой угрозы для безопасности, следует немедленно рассмотреть, оценить и расследовать специально назначенному лицу (лицам) и хранить в отдельной части дела о претензиях.
Результаты расследования и выводы должны быть записаны в средней части бланка для регистрации жалобы потребителя, должна быть подпись ответственного лица и дата проведенной записи.
На основании результатов проведенного расследования должно быть принято решение по дефектному изделию. В нижней части бланка регистрации жалобы должны быть записаны принятые меры по дефектному изделию, подпись ответственного лица и дата.
Это может быть решение по замене изделия(ий), об изъятии всех аналогичных изделий, о внесении изменений в конструкцию изделия или технологию их изготовления. Может быть также решение о признании жалобы необоснованной.
9.5 Первый экземпляр бланка регистрации жалобы потребителей должен храниться в деле службы обслуживания потребителя-покупателя (или в отделе контроля качества), дубликаты должны быть направлены в соответствующие подразделения для принятия безотлагательных мер по устранению дефектов.
На предприятии должны иметься письменные, регулярно проверяемые и пересматриваемые инструкции для того, чтобы быть готовыми к возможному отзыву продукции с рынка.
9.6 На основании полученных рекламаций и проведенным по ним расследованиям, служба обслуживания потребителей должна составлять сводные ведомости дефектов по рекламациям, в которых указывают дату поступления рекламаций, наименование и количество дефектных изделий, дату ответа на жалобу, номер бланка и описание жалобы.
Ежеквартально ведомости должны обрабатываться дня выявления аналогичных жалоб по каждому виду изделий, характеру жалоб, удовлетворению их. Для наглядного представления о количестве рекламаций во времени по видам продукции могут быть построены графики.
Отозванная продукция должна быть промаркирована и должна храниться в отдельном помещении.
Отзыв продукции с рынка должен быть записан в соответствующие журналы.
9.7 Предприятие-изготовитель, располагая только информацией, полученной в результате обработки присланных рекламаций, не может иметь полного представления о качестве своей продукции, т. к. ему известна небольшая часть тех дефектов, которые существуют на самом деле. При таком пассивном сборе информации о производимой продукции, производитель не имеет предложений от потребителя по улучшению качества изделий.
Служба обслуживания должна получать информацию непосредственно с мест эксплуатации изделий, наблюдать за правильностью их использования, давать необходимые консультации, собирать данные о надежности, долговечности и других качественных характеристиках изделий.
Служба обслуживания должна систематически выяснять, в какой степени потребители довольны изделиями их предприятия.
10. Самоинспекция, самооценка деятельности предприятия
10.1 Самоинспекция является важнейшей контрольной функцией предприятия-изготовителя.
Самоинспекция должна решать две основные задачи в достижении надлежащего качества в производстве продукции:
- анализ фактического состояния работы по качеству, выявление всех несоответствий, недоработок, ошибок, нарушений в производственном процессе, в обеспечении качества продукции и требований потребителей;
- недопущение развития их до уровня критических, своевременное принятие корректирующих действий по их устранению, совершенствование деятельности предприятия.
Самоинспекция (самооценка) является для организации способом сопоставить свою деятельность и ее результаты с работой лучшего, конкурирующего предприятия, или модели, отвечающей самым современным представлениям о совершенной организации.
10.2 Принципы работы по организации самоинспекции, самооценки должны заключаться в следующем:
- использование при оценке своей деятельности и ее результатов комплекса критериев, который нашел широкое применение у лучших фирм и предприятий, зарубежных и отечественных;
- систематический подход к совершенствованию деятельности;
- понимание того, что в данной ситуации должно сделать предприятие в целом, его отдельные подразделения и каждый работник на ключевых направлениях;
- получение объективных оценок, основанных на фактах, используя оценку руководителей и отдельных работников;
- выявление и анализ процессов, в которые можно ввести улучшения;
- внедрение различных инициатив и передовых методов управления качеством в повседневную деятельность предприятия;
- возможность распространения передового опыта лучших подразделений предприятия и других предприятий и фирм;
- обучение персонала применению принципов управления качеством;
- возможность признания и стимулирования посредством премирования достижений подразделений и работников.
10.3 Самоинспекция, самооценка должна проводиться на предприятии в соответствии с настоящими Правилами и разработанным планом.
Результаты проведения самоинспекции должны быть документально оформлены с выводами и рекомендациями на устранение недостатков и дальнейшее улучшение работы предприятия.
В проведение работы по самоинспектированию должен быть привлечен широкий круг высококвалифицированных специалистов производства. Участие в этой ответственной работе должно давать им ощущение причастности к важному делу, повышать их чувство ответственности и мобилизовывать на самоконтроль и, в конечном итоге, на коллективный контроль.
Организация, приступающая к самоинспекции, самооценке, должна выбрать такую схему ее проведения, которая будет наилучшим образом соответствовать потребностям, структуре и опыту этой организации.
Самооценка может быть проведена в целом по предприятию, может быть инициирована для отдельного подразделения или какого-либо отделения.
10.4 Руководители предприятия принимают решение о проведении самооценки. Назначается руководитель проекта, который должен возглавить работу по самооценке, включая составление отчета, то есть обобщение всей собранной информации и представление отчета в готовом виде.
Назначаются руководители подразделений, ответственные за проведение самооценки по одному или нескольким конкретным критериям.
Руководители подразделений назначают конкретных работников для участия в работе группы.
Члены группы или изучают методы самооценки самостоятельно, или проходят обучение под руководством экспертов, имеющих специальную подготовку.
10.5 На предприятии должны иметься письменные инструкции по проведению самоинспекции. Они должны включать следующие основные вопросы:
- персонал;
- помещения, включая помещения для подготовки персонала;
- эксплуатация зданий и оборудования;
- хранение сырья и готовых продуктов;
- контроль производства и постадийный контроль;
- контроль поступления, хранения и использования упаковочных и маркировочных материалов;
- контроль качества;
- документация,
- санитария и гигиена;
- совершенствование технологических процессов;
- программы по проведению валидации и ревалидации;
- калибровки инструментов и измерительных приборов;
- конкурентоспособность;
- процедура отзыва продуктов с рынка, обучение потребителей;
- порядок рассмотрения рекламаций, уровень дефектности;
- результаты проведения предыдущих самоинспекций и принятые меры.
Члены группы собирают данные и формируют разделы отчета по закрепленным за каждым из них критериям или их составляющим.
Составители представляют сводный отчет руководителю предприятия.
Руководитель предприятия рассматривает, вносит корректировки и утверждает отчет как документ, дающий объективное представление о состоянии дел на предприятии.
Частота проведения самоинспекций должна определяться самим предприятием.
10.6 В числе объектов самооценки, кроме вышеперечисленных может быть информация о том, как организация изучает, прогнозирует и улучшает удовлетворенность общества своей деятельностью, в том числе, по таким аспектам, как:
деятельность, относящаяся к:
- охране труда и безопасности;
- удовлетворенности условиями работы;
- снижение риска заболеваний и уровня травматизма;
- загрязнениям и вредным выбросам, шуму;
- текучести персонала;
- определению и сочетанию способностей людей с поставленными целями;
- разработке и реализации планов обучения персонала;
- развитию способностей людей;
- обучению приемам, развитию умения работать;
- обеспечению непрерывности обучения работников;
- анализу эффективности обучения;
- подаче предложений по улучшению качества;
- обеспечению возможности принятия персоналом мер по улучшению качества и оценке их эффективности;
- поддержанию участия отдельных работников, групп и подразделений в процессе улучшения качества;
- созданию системы поощрения вовлеченности в работы по качеству;
- психологическому климату в коллективе, отношению со стороны руководства, отношения в коллективе, рабочей обстановке.
ПРИЛОЖЕНИЯ
Приложение 1
Схема потоков основных процессов изготовления медицинских изделий из полимерных материалов
Приложение 2
Схема потоков основных процессов изготовления медицинских изделий из тканых и нетканых материалов
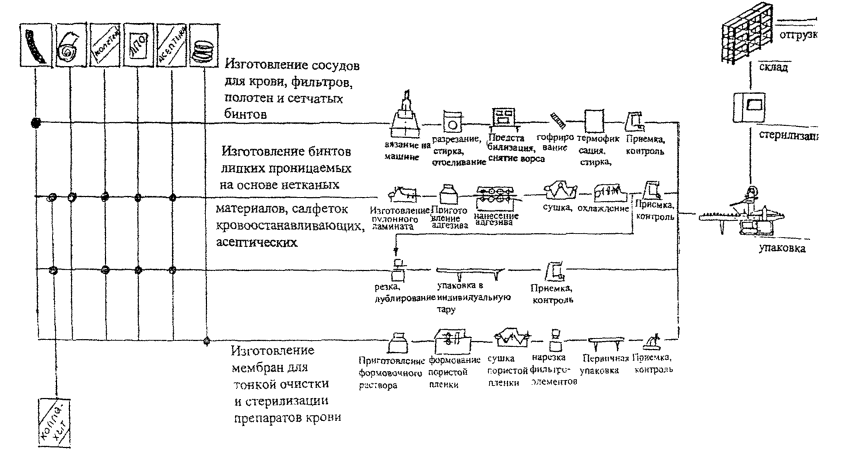
Приложение 3
Методика определения механических частиц в воздухе помещений производств изделий медицинского назначения из полимерных материалов
Методика определения механических частиц в воздухе предназначена для контроля чистоты воздуха в чистых помещениях производств изделий медицинского назначения из полимерных материалов. Чистые помещения - это помещения, в которых осуществляются производственные процессы, связанные с выпуском стерильной продукции, с нормируемыми показателями чистоты воздуха по содержанию механических частиц и микроорганизмов, с регулированием температуры, влажности и давления воздуха.
Под механическими частицами подразумеваются частицы полидисперсного состава (пыль, аэрозольные частицы, микроорганизмы и т.п.), содержащиеся в воздухе.
Контроль воздуха на содержание механических частиц необходимо осуществлять не менее одного раза в неделю.
1. Средства измерения и вспомогательные устройства
1.1 Фотоэлектрический счетчик АЗ-5.
1.2 Трубка резиновая с внутренним диаметром 0,008 м, длиной (1,0 ± 0,1) м.
1.3 Секундомер.
1.4 Ткань безворсовая.
1.5 Спирт этиловый.
2. Метод измерения
Определение механических частиц в воздухе основано на применении фотоэлектрического счетчика частиц АЗ-5. Работа прибора основана на рассеянии света отдельными частицами. Каждая частица генерирует в оптическом датчике электрический импульс, амплитуда которого пропорциональна размеру регистрируемой частицы.
Прибор АЗ-5 позволяет измерять концентрации частиц с размером 0,4 - 10 мкм от единицы до 300000 частиц в одном литре исследуемого воздуха.
Прибор АЗ-5 рассчитан на эксплуатацию при относительной влажности воздуха до 80 % и температуре от 10 до 35 °С.
3. Правила безопасности
3.1 Фотоэлектрический счетчик АЗ-5 предназначен для обслуживания лицом, имеющим право работать с переносными измерительными приборами общего назначения.
3.2 При работе с прибором необходимо соблюдать «Правила техники безопасности при работе с радиотехническим оборудованием».
3.3 Прибор должен быть заземлен через клеммы на задней панели, знак заземления по ГОСТ 21130-75.
4. Условия выполнения измерений
Измерения выполняются в помещениях с нормальным и небольшим избыточным давлением (до 30 Па).
5. Подготовка к выполнению измерений
5.1 Проверяют питающее напряжение прибора. Для этого нажимают кнопку «Контроль», находящуюся на задней панели прибора. Стрелка прибора должна отклониться в пределах закрашенного сектора при включенном насосе.
Время самопрогрева прибора (60 ± 5) с. При длительном бездействии прибора время самопрогрева прибора - не менее 30 мин.
5.2 Проверяют чувствительность прибора - производят калибровку прибора согласно «Инструкции по эксплуатации».
5.3 Перед подачей прибора в чистые помещения его протирают салфеткой из безворсовой ткани по ГОСТ 12087-77, артикул 82138, смоченной в 76 %-ном растворе этилового спирта по ГОСТ 5962-67, снимают крышки на приборе и защитный колпачок со штуцера «вход аэрозоля».
6. Выполнение измерений
6.1 В чистом помещении выбирают точки отбора проб воздуха.
Количество точек отбора определяется площадью помещения (см. схемы отбора). Отбор проб воздуха осуществляют не менее трех раз из одной точки.
В помещении площадью не более 15 м2 - 1 точка (отбор пробы в точке 1).
В помещениях площадью от 15 м2 до 100 м3 - 2 точки (отбор пробы в точках 2 и 5).
В помещениях площадью более 100 м2 - 5 точек отбора (отбор пробы в точках 1, 2, 3, 4, 5).
В узких и длинных помещениях - 3 точки отбора (точки 1, 2, 3), на расстоянии не более 5 м друг от друга.
Схема отбора проб в помещении площадью от 15 м2

Схема отбора пробы в длинном помещении
|
1 |
2 |
3 |
- |
- |
6.2 Измерение высоких концентраций частиц.
Для измерения высоких (более 250 частиц/л) концентраций частиц используется канал непрерывного измерения.
6.2.1 Включают прибор в сеть. Переключатель диапазонов концентрации частиц устанавливают в положении «300». Непосредственно перед измерением включают тумблер «вкл». При этом загорается индикаторная лампа (зеленая). После минутного самопрогрева прибора на штуцер «вход аэрозоля» надевают фильтр Ф из комплекта прибора. Включают насос тумблером «насос». Устанавливают скорость аспирации 1,2 л/мин и прокачивают воздух в течение 10 мин.
Отключают насос, снимают фильтр. После этого приступают к измерению.
6.2.2 Для определения количества частиц регистрируемого размера в 1 л воздуха переключатель размера частиц устанавливают на регистрируемую величину (0,5 мкм или 4 мкм) и включают насос, поддерживая скорость аспирации, равной 1,2 л/мин в течение не менее 1 мин.
Переключатель диапазонов концентрации частиц устанавливают в такое положение, чтобы стрелка прибора находилась около или правее середины шкалы. При такой установке концентрация частиц в 1 л воздуха измеряется наиболее точно.
6.2.3 Отсчет производят по шкале показывающего прибора с учетом установленного диапазона измерений.
6.3 Измерение низких концентраций частиц.
6.3.1 Для измерения собственного фона прибора на штуцер «вход аэрозоля» надевают фильтр Ф из комплекта прибора, включают насос и в течение 15 мин откачивают воздух из камеры анализатора. Включают насос и включают электромеханический счетчик нажатием кнопки дозированного измерения на время (50 ± 1) с. Загорается индикаторная лампочка (красная). Показания снимают при погасшей лампочке.
При величине регистрируемых частиц 0,5 мкм и более фон должен быть не более фона не должно быть.
6.3.2 Для измерения низких концентраций включают насос, устанавливают скорость аспирации 1,2 л/мин, устанавливают переключателем регистрируемую величину частиц и включают механический счетчик.
Запускают счетчик нажатием кнопки дозированного измерения на время не менее 1 с. При этом на (50 ± 1)с загорается индикаторная лампочка (красная). Счетчик включается автоматически и сохраняет показания, которые снимают после того, как погаснет индикаторная лампа.
Сброс показаний осуществляется нажатием клавиши сброса.
6.3.3 Собственный фон прибора вычитают из показаний счетчика.
7. Обработка результатов измерений
Количество частиц в контролируемой точке определяют как среднее арифметическое из трех измерений для каждой из величин регистрируемых частиц.
Количество частиц в 1 л воздуха в контролируемой точке определяется по формуле (1):
где ni - i измерение в контролируемой точке;
Р - количество измерений.
Количество частиц в 1 л воздуха в помещении определяется по формуле (2):
где nj - количество частиц в 1 л воздуха в j точке;
q - количество точек.
8. Оформление результатов
Результаты замеров количества частиц в помещениях заносят в таблицу рабочего журнала.
|
№ п/п |
Дата |
Наименование помещения |
Размер частиц |
Показание прибора |
Количество частиц в 1 л воздуха в контролируемой точке |
Содержание частиц в 1 л воздуха в помещении |
||||
|
т. 1 |
т. 2 |
т. 3 |
т. 4 |
т. 5 |
||||||
|
|
|
|
0,5 мкм и более |
|
|
|
|
|
|
|
|
|
|
|
4 мкм и более |
|
|
|
|
|
|
|
Приложение 4
Методика определения инициальной контаминации продукции, стерилизуемой радиационным способом
Утверждена зам.
Главного государственного санитарного врача СССР
В.Е. Ковшило (№ 2535 - 82 от 11.02.1982 г.)
1. Общие положения
1.1 Инициальная контаминация характеризуется средним числом жизнеспособности микроорганизмов, обсеменяющих единицу готовой продукции.
1.2 Контаминированность продукции до стерилизации зависит от технологии процесса и санитарно-гигиенических условий на производстве.
1.3 Предельно допустимые показатели инициальной контаминации устанавливаются для каждого конкретного вида радиационно стерилизуемой продукции соответствующим нормативно-техническим документом на эту продукцию.
1.4 Предприятия, выпускающие изделия, стерилизуемые радиационным способом, осуществляют постоянный контроль инициальной контаминации продукции.
2. Определение инициальной контаминации
2.1 Определяется инициальная контаминация каждой партии изделий. Партией считается количество продукции, изготовленной в течение суток, начиная с 24 часов.
2.2 Отбор проб для определения инициальной контаминации проводят в соответствии с таблицей.
Отбор проб для определения инициальной контаминации изделий
|
Количество изделий в партии |
Количество изделий, отбираемых на анализ |
|
До 100 |
2 - 4 |
|
1000 |
3 - 6 |
|
3000 |
4 - 8 |
|
5000 |
5 - 10 |
|
6000 |
6 - 12 |
|
7000 |
7 - 14 |
|
10000 |
10 - 20 |
Если в партии содержится более 1000 изделий,
то отбор проб производится по формуле ![]() , где n - количество изделий, выпущенное за сутки,
при минимальном количестве проб - 2 и максимальном - 40.
, где n - количество изделий, выпущенное за сутки,
при минимальном количестве проб - 2 и максимальном - 40.
2.3 Пробы отбираются работниками бактериологической лаборатории или работниками отдела технического контроля предприятия - изготовителя.
2.4 Инициальную контаминацию определяют в микробиологическом боксе, находящемся в обычном лабораторном помещении.
2.5 В предбокснике изделия освобождают от внешней упаковки, помещают в стерильный лоток и вносят в бокс.
2.6 Смыв производится только с рабочих поверхностей изделий. В качестве смывной жидкости используют стерильный физиологический раствор хлорида натрия с добавлением 0,1 % твина-80. Объем смывной жидкости должен примерно соответствовать 10-кратному объему обрабатываемого изделия. Для обработки шовных материалов и перевязочных средств смывная жидкость берется в количествах достаточных для полного погружения объектов при встряхивании на шуттель-аппарате. Встряхивание производят в течение 10 минут.
2.6.1. Для подсчета количества жизнеспособных микроорганизмов в смывной жидкости используются 2 способа: путем фильтрации через мембранные фильтры или непосредственным высевом на плотную питательную среду. Для фильтрации используют аппараты, выпускаемые промышленностью, позволяющие задерживать на поверхности мембранного фильтра все микроорганизмы, содержащиеся в смывной жидкости.
Величина пор таких мембран составляет ≤ 0,32 мкм.
По окончании фильтрации мембраны помещают внутренней (гладкой) поверхностью на плотную питательную среду в чашки Петри и инкубируют в течение 48 часов при 32 °С.
При необходимости определять анаэробную микрофлору (в кетгуте) часть мембранных фильтров инкубируют в анаэробных условиях в течение 48 часов при 37 °С. Выросшие колонии подсчитывают визуально или с помощью лупы. Количество выросших колоний соответствует количеству микроорганизмов в объеме профильтрованной через мембрану смывной жидкости.
2.6.2 При прямом посеве смывной жидкости в питательную среду, в зависимости от предполагаемой инициальной контаминации, засеивают 0,5 мл смывной жидкости на поверхность питательного агара (разлитого в чашки Петри и предварительно подсушенного) или 1,0 - 2,0 мл в толщу агара. В последнем случае определенный объем смывной жидкости вносят пипеткой в стерильные чашки Петри, затем вливают в них 15 - 20 мл расплавленного и остуженного до 45 - 50 °С питательного агара, круговыми движениями на ровной гладкой поверхности вращают чашки Петри в течение 30 - 45 секунд, перемешивая жидкость и агаризованную среду для равномерного распределения в ней микроорганизмов, оставляют чашки на ровной поверхности до застывания агара, после чего инкубируют при 32 °С в течение 48 часов. Зная количество физиологического раствора, использованного для смыва, объем засеянной жидкости и количество изделий, определяют инициальную контаминацию одного изделия.
Из показателей инициальной контаминации каждого образца устанавливают среднюю величину, характеризующую инициальную контаминацию данной партии продукции.
Приложение 5
Методика обнаружения радиорезистентных микроорганизмов на предприятиях медицинской промышленности, выпускающих радиационно стерилизуемую продукцию
Методика включает три этапа работы: выделение на производстве с помощью обычных методов смешанной микрофлоры, облучение смешанной популяции суббактерицидными дозами ионизирующих излучений с целью селекции радиорезистентных микроорганизмов и качественное определение радиорезистентности у микроорганизмов после радиоселекции.
1. Выделение производственной микрофлоры проводится в цехе окончательной сборки и упаковки продукции ватными тампонами, а также из оптовой продукции путем смыва. Одним тампоном, увлажненным физиологическим раствором, в который рекомендуется добавить 1 % твина-80, протирают поверхность оборудования и рабочих мест площадью 0,2 м2. Смывы с изделий производят так же, как и при определении их инициальной контаминации. Одновременно используют 5 тампонов и выборку изделий, равную удвоенной выборке, используемой для определения инициальной контаминации.
Тампоны встряхивают в течение 10 мин в пробирках с 5 до 0,9 % раствора хлорида натрия. Смывную жидкость смешивают и фильтруют через мембранный фильтр (размер пор 0,3 мкм; диаметр диска предпочтительно 60 мм). 0,1 мл неотфильтрованной смывной жидкости высевают в разведениях 1:100 - 1:10 на плотную питательную среду (МПА, агар Хоттингера, 75 % аминного азота, РН 7,0 - 7,2) методом заливки для подсчета числа жизнеспособных клеток в испытуемой жидкости. Учет результатов высева проводят через 18 - 24 ч после инкубации при 39 °С.
Смыв с изделий смешивают и обрабатывают так же, как и смывную жидкость с тампонов.
Фильтры по окончании фильтрации высушивают в боксе на открытом воздухе при комнатной температуре и отключенных бактерицидных лампах в течение 12 - 18 часов.
Пригодными для дальнейшей работы считаются фильтры, через которые профильтрована испытуемая жидкость, содержащая в целом не менее 103 микроорганизмов (данные о содержании микроорганизмов находят путем пересчета результатов высева, с учетом общего объема профильтрованной жидкости, разведения и объема инокулянта).
3. Качественное определение радиорезистентности микроорганизмов, выделяемых из смешанной популяции после облучения.
Выросшие на фильтре после облучения колонии пересеивают в пробирки со скошенным агаром (пункт 2), инкубируют при 32 °С в течение 18 - 24 час, а для спорообразующих микроорганизмов после инкубации в термостате дополнительно выдерживают в затемненном помещении при комнатной температуре 7 дней, и готовят по оптическому стандарту мутности на 10 ед. взвеси путем смыва физиологическим раствором микробной массы. 0,1 мл этой взвеси переносят в пробирку с 0,9 мл стерильного 0,9 % раствора хлорида натрия и облучают в дозе 3,5 Мрад. После облучения в пробирку с соблюдением правил асептики добавляют 9 мл бульона Хоттингера или МПБ, посевы инкубируют в течение 7 дней. Наличие роста свидетельствует о высокой радиорезистентности данного микроорганизма. Количественно определить радиорезистентность можно по показателям Д10 (дозы облучения, при которых численность популяции микроорганизмов уменьшается в 10 раз). Высокорезистентными считаются микроорганизмы, для которых показатели Д10 равны или превышают 500 крад. Такие микроорганизмы встречаются в окружающей среде весьма редко (10-4). При обнаружении с помощью описанной методики следует улучшить соблюдение на производстве санитарно-гигиенического режима, а также при необходимости провести дополнительные санитарно-гигиенические мероприятия.
Контроль радиорезистентности производственной микрофлоры по изложенной методике рекомендуется проводить один раз в квартал.
Все выделенные штаммы микроорганизмов с положительным результатом качественного теста на радиорезистентность направляются для количественного определения радиорезистентности этих микроорганизмов в учреждении, в котором проводятся радиобиологические исследования (Институт биофизики Министерства здравоохранения СССР, Институт эпидемиологии и микробиологии им Н.Ф. Гамалеи АМН СССР, ВНИИ дезинфекции и стерилизации Минздрава СССР).
Приложение 6
Порядок
обработки и дезинфекции помещений
(объем работ ежемесячного санитарного дня)
Влажную уборку с дезинфекцией в чистых производственных помещениях проводят после остановки производства для проведения ремонтных работ, в случае обнаружения в воздухе, на строительных элементах и оборудовании спорообразующей микрофлоры и грибов свыше допустимых величин, но не реже 1 раза в месяц.
Должен соблюдаться следующий порядок проведения и объем выполняемых работ:
- из помещения удаляют отходы производства и неиспользованные материалы, а продукцию и полуфабрикаты накрывают пленкой;
- выключают вытяжную и приточную вентиляции, обеспечивают лампы освещения и оборудования;
- удаляют пыль с инженерных коммуникаций, ламп освещения и т.д.;
- потолок, стены, окна, двери, стеллажи, оборудование, нетоковедущие части осветительных и бактерицидных ламп, столы, стулья и т.д., моют дезраствором при помощи перкалевых салфеток или безворсовых тряпок. Наиболее загрязненные места моют наиболее тщательно;
- двери, окна, стены и перегородки, стеллажи обильно смачивают дезрастворами или орошают из гидропульта с помощью турбулирующей аэрозольной насадки;
- после этого помещение закрывают на 35 - 45 мин. Затем удаляют с обработанных поверхностей остатки жидкости безворсовой тканью и моют пол;
- работы производить согласно рабочим инструкциям; операции, связанные с обильным применением резиновых перчаток, сапог, фартуков, а при необходимости защищать рот и нос 4-слойной марлевой повязкой.
Приложение 7
Порядок обработки и дезинфекции вентсистемы
Дезинфекцию фильтрокамер и воздуховодов вентиляционных установок чистых производственных помещений проводят в случае ремонта воздуховодных линий, смены фильтров тонкой очистки, обнаружения микрофлоры в приточных вентсистемах, а также 1 раз в год по графику, утвержденному на предприятии.
Предлагается следующий порядок проведения и объем выполняемых работ:
- произвести очистку внутренних и наружных поверхностей фильтрокамер и воздуховодов вентиляционных установок от механических загрязнений;
- промыть горячей водой с температурой 50 - 60 °С;
- произвести обработку дезинфицирующим раствором, содержащим 0,5 % моющего средства и 6 % перекиси водорода, путем его распыления или мойкой поверхности. В качестве дезинфицирующего раствора для корродирующих элементов применять 0,05 % раствор цетилперидиний бромида с последующей протиркой 76 % этиловым спиртом;
- через 2 часа произвести удаление излишней жидкости, протирку поверхностей дистиллированной, обессоленной или деионизированной водой;
- привести воздуховодную линию в рабочее состояние и поставить формалиновую баню с целью дезинфекции ее труднодоступных участков.
(Формалиновые бани ставят только в отсутствии людей в рабочих помещениях следующим образом:
- наливают 1 - 4 литра (в зависимости от микрофлоры) 16 % формалина в контейнер;
- устанавливают контейнер в промежуточную камеру);
- включают приточную и вытяжную вентиляции. Продолжительность бани от 10 мин до 1 часа, в зависимости от количества формалина (см. выше). После окончания дезинфекции контейнер убирают из камеры. Работу в помещении после постановки формалиновой бани начинают по истечении не менее 4 часов работы систем вентиляции.
При постановке формалиновой бани необходимо пользоваться резиновыми перчатками, сапогами, фартуком, противогазом марки А, а работы производств - согласно рабочим инструкциям.
Приложение 8
Контроль микробной обсемененности поверхностей оборудования и помещений
Определение микробной обсемененности должно проводиться выборочно не реже одного раза в неделю во время производственного процесса и за 1,5 часа до начала работы.
Микробиолог, определяющий микробную обсемененность поверхностей оборудования и помещений, должен работать в стерильной технологической одежде и перчатках.
Контроль микробной обсемененности аппаратуры, оборудования и коммуникаций проводится с помощью смывов стерильными тампонами.
Стерильные ватные тампоны готовят предварительно на стеклянных или металлических палочках, вмонтированных в ватно-марлевые пробки пробирок. Пробирки должны содержать приблизительно по 2 мл стерильного 0,9 % раствора хлорида натрия. На месте взятия смыва тампон увлажняют наклоном пробирки.
Для получения смыва увлажненным тампоном проводят по поверхности аппаратуры или коммуникаций с площадью 100 см2, ограниченной стерильной рамкой-трафаретом. Смывы с мелких предметов берут со всей поверхности. Количество проб зависит от величины исследуемого объекта.
После взятия пробы тампоном проводят несколько раз по поверхности чашки Петри с мясо-пентонным агаром или агаром, приготовленным из панкреатического гидролизата мяса глубокого расщепления (120 мг % аминного азота, РН 7,2 - 7,3) в двух чашках Петри. Возможно использование питательных сред, приготовленных из сырья непищевого назначения.
Чашки Петри помещают в термостат и выдерживают при 24 °С и 37 °С в течение 48 часов, после чего проводят подсчет выросших микроорганизмов.
В смывах с площади 10×10 см2 допустим рост не более 10 колоний неспорообразующих микроорганизмов на двух параллельных чашках.
Результаты контроля фиксируются в журналах по каждому чистому помещению в отдельности.
Приложение 9
Контроль микробной обсемененности рук персонала
Определение микробной обсемененности рук персонала должно проводиться один раз в неделю во время работы выборочно у нескольких работающих в каждом чистом помещении.
В лаборатории готовят ватные тампоны на стеклянных или металлических палочках, вмонтированных в ватно-марлевые пробки пробирок. Пробирки должны содержать приблизительно по 2 мл стерильной дистиллированной воды.
На месте взятия смыва тампон увлажнить наклоном пробирки. Для получения смывов с рук увлажненным тампоном тщательно протереть ладони, тыльные стороны кисти, между пальцами, ногти обеих рук. Использовать по 2 тампона на одного человека (по одному тампону на каждую руку).
После взятия пробы каждым тампоном несколько раз провести по поверхности МПА или агара, приготовленного из панкреатического гидролизата мяса глубокого расщепления (120 мг % аминного азота, РН 7,2 - 7,4) в двух чашках Петри. Возможно использование питательных сред, приготовленных из сырья непищевого назначения, способствующего выявлению роста микроорганизмов.
Предварительно чашки выдержать при 37 °С в течение 24 часов, проросшие чашки бракуются.
После отбора проб чашки Петри поместить в термостаты и выдержать при 24 °С и 37 °С в течение 48 ч.
После окончания инкубации произвести подсчет числа выросших колоний микроорганизмов.
На руках после обработки не должны содержаться микроорганизмы. В процессе работы допускается наличие не более 2 колоний неспорообразующих микроорганизмов в смывах с рук одного рабочего.
Микробиолог, определяющий микробную обсемененность рук, должен работать в стерильной технологической одежде и перчатках.
Результаты контроля фиксируются в журналах для всех работающих по каждому чистому помещению в отдельности.
Приложение 10
Принципы менеджмента качества
В международных стандартах ИСО 9000, разработку и пересмотр которых осуществляет технический комитет ИСО/ТК 176 «Общее руководство качеством и обеспечение качества» сформулированы задачи планирования качества.
В соответствии с ними, планирование качества включает работы, в процессе которых выявляются цели и требования к качеству, а также к применению необходимых элементов систем качества. Планирование качества охватывает планирование производства, планирование управленческих и оперативных мероприятий, планирование улучшения качества.
Стандарты ИСО 9000-2000 (новой версии) имеют общую структуру, основанную на модели процесса менеджмента качества.
Стандарт ИСО 9001-2000 ориентирован на требования к системе качества предприятия и на демонстрацию возможностей его по обеспечению качества продукции, соответствующего требованиям потребителя.
Положения стандарта ИСО 9001-2001 пригодны для адаптации, в него включены требования, предусматривающие постоянное улучшение и предупреждение несоответствий.
Стандарт ИСО 9004-2000 содержит методические указания по менеджменту качества и постоянному улучшению процессов, которое способствует удовлетворению всех заинтересованных сторон потребителей, работающих, поставщиков и общества в целом.
Согласованная пара стандартов ИСО 9001 и ИСО 9004 может быть применена ко всем общим категориям продукции и обеспечивает основу для требований, которые могут быть разработаны конкретными отраслями и отдельными предприятиями.
Стандарт ИСО 9004 ориентирован на достижения результативности в деятельности предприятия в интересах потребителя и общества в целом и представляет методическую помощь по всем аспектам системы качества с целью улучшения эффективности деятельности предприятия.
Стандарт рекомендует принять для менеджмента качества принцип «подхода как к процессу».
Модель процесса менеджмента качества представлена на рисунке 1.
Любая деятельность, получающая входные данные и преобразующая их в выходные, может рассматриваться как процесс. Для успешного функционирования предприятия необходимо определить многочисленные взаимосвязанные процессы и управлять ими.
Принципы менеджмента качества заключаются в следующем:
I Ориентация на потребителя
Предприятие должно знать настоящие и перспективные запросы своих потребителей, обеспечить выполнение их требований и стремиться превзойти их ожидания.
Детально указанный принцип заключается в следующем:
- знание и понимание потребностей и ожиданий потребителя таких, как качество продукции, ее цена, безопасность, надежность и удобство пользования, режим поставки;
- моделирование потребностей потребителя, тесный контакт с ним (включая жалобы);
- доведение этих потребностей до всех работающих на предприятии;
- оценка удовлетворенности потребителей и корректирующие действия;
- управление взаимодействия с потребителями;
- обеспечение сбалансированного подхода к запросам сторон (поставщиков, регионов и общества в целом).
II Ответственность и роль руководства
Руководители должны создать единство целей предприятия и его управления. Они должны обеспечить понимание всем персоналом целей предприятия в обеспечении качества и вовлечение его в достижение поставленных целей.
Указанный принцип заключается в следующем:
- разработка политики и целей в области качества, разработка руководства по качеству;
- обеспечение поддержки всего персонала, участие его в обеспечении качества, совершенствования технологий, повышения квалификации, анализа требований потребителей;
- обеспечение персонала необходимыми ресурсами, свободы действий в рамках ответственности;
- персональная ответственность руководства за каждую функцию управления качеством;
- обеспечение атмосферы доверия, инициирования и поощрения инициативы работников;
- обучение, «выращивание» работников;
- поддержание связей с внешними сторонами по вопросам системы качества поставщиков;
- анализ системы через определенные промежутки времени;
- определение прогноза будущего предприятия.
III Персонал организации - активное начало в обеспечении качества
Работники всех уровней составляют сущность предприятия, вовлечение их в процесс производства дает возможность использовать их способности и потенциал на благо предприятия.
Указанный принцип заключается в следующем:
- принятие инициативы и ответственности в решении проблем;
- активный поиск возможностей улучшения, поиск недостатков и ошибок в работе системы;
- поиск возможностей повышения уровня своих знаний, опыта и компетентности;
- передача своего опыта и знаний сотрудникам;
- создание дополнительных ценностей для потребителей;
- представление своего предприятия потребителям и всем, заинтересованным в положительном свете;
- получение удовлетворения от работы, испытывание чувства гордости за свою работу.
IV Принцип «подхода как к процессу»
Для успешного функционирования предприятия, эффективного достижения желаемого результата необходимо определение многочисленных взаимосвязанных процессов и управление ими; систематическая идентификация и менеджмент процессов и взаимодействие между такими процессами могут считаться «подходом как к процессу».
Принцип заключается в следующем:
- определение процесса для достижения желаемого результата;
- оценка и сбор данных, идентификация и измерения входов в процесс и его результатов;
- оценка проектной документации и перспектив предприятия;
- оценка рисков, последствий и влияния процесса на потребителей и заинтересованные стороны, корректирующие действия;
- установление прав, полномочий и ответственности за управление процессом;
- определение потребителей, поставщиков и других заинтересованных сторон;
- планирование качества;
- рассмотрение проектирования на всех этапах, их ресурсного обеспечения, потребностей в обучении.
V Системный подход к менеджменту
Эффективность и результативность предприятия повышаются при понимании и управлении системой взаимосвязанных процессов в соответствии с установленной целью.
Принцип заключается в следующем:
- разработка или планирование процесса путем установления и разработки системы процессов, обеспечивающих достижение заданных целей;
- проектирование такой системы, при которой цель достигается наиболее эффективным путем;
- определение взаимозависимости процесса в системе;
- постоянное улучшение системы через измерения и оценку;
- определение ресурсных возможностей.
VI Принцип постоянного улучшения
Постоянной целью предприятия должно быть непрерывное улучшение.
Принцип заключается в следующем:
- формирование потребности у каждого работника предприятия в постоянном улучшении продукции, процессов и системы в целом;
- постоянное повышение эффективности процессов;
- периодическая оценка соответствия установленным критериям, совершенствование для определения области потенциального улучшения;
- обучение каждого работника методам и средствам постоянного улучшения;
- определение меры и целей организации улучшения;
- признание и поощрение улучшений.
VII Метод при принятии решения, основанный на фактах
Эффективные решения основываются на анализе данных и информации.
Принцип заключается в следующем:
- измерение и сбор данных и информации, относящихся к задаче;
- уверенность в достоверности и точности данных информации;
- использование апробированных методов для анализа данных и информации;
- выбор соответствующих статических методов обработки информации;
- принятие решений и действия на основе результатов анализа, опыта и инструкции.
VIII Взаимовыгодные отношения с поставщиками
Предприятие и его поставщики взаимозависимы, и взаимовыгодные отношения увеличивают способность обеих сторон создавать ценности. Принцип заключается в следующем:
- идентификация основных поставщиков;
- установление отношений на основе баланса краткосрочных и долгосрочных целей предприятия и общества;
- организация четких и открытых связей;
- совместная работа по четкому пониманию запросов потребителя;
- инициирование совместных разработок и улучшение продукции и процессов;
- обмен информацией и планами на будущее;
- признание достижений и улучшений продукции поставщика;
- создание атмосферы добросовестного партнерства.
Приложение 11
Контроль производственного процесса
Контролю производственного процесса отведено видное место в стандартах по обеспечению качества. В стандарте ИСО 9001 этому вопросу посвящен раздел, в нем установлено, что изготовители должны планировать производство, определять процессы, которые непосредственно влияют на качество и подтверждать, что они проводятся в контролируемых условиях.
Наиболее важные с точки зрения обеспечения качества работы в области производственного контроля представлены в таблице.
Таблица
|
Виды работ |
Состав работ |
Кем выполняется |
Действия по обеспечению качества |
|
Рассмотрение требований контракта (требований заказчика) |
Определение масштаба и характера работ. Рассмотрение стандартов, ТУ и спецификации применительно к продукции. Рассмотрение требований применяемого исходного сырья, материалов и полуфабрикатов; Оценка источников их поставок. Рассмотрение и установление требований к контролю технологического процесса и испытания к продукции. Составление плана контроля и испытаний. |
Руководство предприятия-изготовителя (представитель руководства), отдел контроля качества, руководители производства. |
Проконтролировать, что факты отсутствия необходимой информации или наличия неточной информации установлены и доведены до ответственных лиц. |
|
Разработка необходимой документации |
Определение политики в области качества и разработка руководства по качеству. Разработка документов по определению функций ответственности полномочий руководителей и работников. Разработка документации, охватывающей - описание производственного процесса (регламента); - рабочих инструкций; - планов контроля испытаний; - методик испытаний; - валидацию производства; - инструкций по технике безопасности и производственной санитарии; - пожарной безопасности; - сертификации производства и др. - разработка документов, определяющих порядок подготовки, утверждения, распределения документов, внесения изменений в них, сохранению, изъятию и отмене документов. |
Руководство предприятия. Руководители производственных служб, отдел контроля качества. |
Проверить разработку документации. |
|
Контроль и поверка измерительного и испытательного оборудования |
Составление графиков обслуживания, поверки, ремонта и наладки оборудования. Разработка компьютерных программ, картотек, специальных журналов. |
Руководство предприятия, специализированные службы. |
Проверить разработку графиков, картотек, компьютерных программ. |
|
Контроль входного сырья, материалов и полуфабрикатов |
Проверка адекватности основных источников поставки сырья, материалов и полуфабрикатов. Проверка сырья, материалов и полуфабрикатов на соответствие требованиям нормативно-технической документации. Документирование результатов входного контроля. Обеспечение и контроль условий хранения сырья, материалов и полуфабрикатов. Принятие мер по выяснению причин брака сырья, материалов и полуфабрикатов и предотвращения повторения его. |
Руководство отдела снабжения. Отдел контроля качества. Руководство производства. |
Проверить документацию (записи). Проверить выполнение заданий. |
|
Контроль технологического процесса |
Изучение, анализ, поддержание в рабочем состоянии и своевременное внесение изменений во все документы, обеспечивающие технологический процесс производства продукции. Использование соответствующего (подходящего) производственного оборудования и контрольно-измерительных приборов, а также подходящей производственной среды. Проверка соответствия ведения процесса программе качества, технологической, нормативно-технической документации, правилам и нормам, принятым для производства. Управление и контроль соответствующими параметрами технологических этапов, процесса в целом. Документирование (текущее) процессов производства и контроля. Соответствующее техническое обслуживание, ремонт и наладка оборудования для обеспечения возможностей непрерывного процесса. Обеспечение и контроль окружающей среды. Обеспечение хранения продукции. |
Отдел контроля качества. Руководство предприятия, руководители производства и обслуживающих отделов. |
Проверить документацию. Проверить соблюдение плана контроля и испытаний. |
|
Контроль готовой продукции |
Испытание продукции в соответствии с планом контроля и испытаний. Изучение и наличие необходимой для контроля документации: - нормативно-технической документации; - сертификаты на входное сырье; - результаты измерений; - результаты функциональных испытаний; - результаты неразрушающего контроля; - результаты приемо-сдаточных и периодических испытаний и т.д. Обеспечение надлежащих объемов выборки продукции для контроля. |
Отдел контроля качества. |
Проверить соблюдение плана контроля. |
|
Статус контроля и испытаний |
Официальное документированное удостоверение соответствия или несоответствия установленным требованиям испытаний (проконтролированной продукции) |
Отдел контроля качества. |
Проверить документацию. |
|
Идентификация и прослеживаемость |
Разработка системы идентификации, которая указывала на состояние изделия в процессе (ожидает контроля, проверено, забраковано) и процедуры обеспечения маркирования и этикетирования сырья, материалов, комплектующих, готовой и промежуточной продукции, а также технической и технологической документации на них. |
Отдел контроля качества, руководители производств. |
Проверить соблюдение плана, контроля и процедуру маркирования. |
|
Сохранность, упаковка, отгрузка и поставка |
Документированное оформление условий хранения, упаковки, отгрузки и поставки продукции. Обеспечение соответствующего оборудования, методов, обеспечивающих гарантировано сохранность продукции в указанных операциях. |
Отдел контроля качества, руководители отдела снабжения и служб. |
Проверить документацию. |
|
Анализ и утилизация продукции, не соответствующей ТУ. |
Разработка документа по выбраковке продукции, ответственного за принятие решения забракования изделий и по утилизации брака. |
Руководители производств, отдел контроля качества. |
Проверить документацию. |
|
Аудит и корректирующие действия |
Изучение всех регистрируемых данных по обеспечению качества. Выработка действий по устранению причин несоответствия продукции НТД, предупреждающих повторение дефектов, по профилактике и предупреждению повторения брака. Изучение отчетов по использованию продукции и рекламаций потребителя. |
Руководство предприятием, отдел контроля качества. |
Рассмотреть результаты аудита и документацию. |
|
Обучение и подготовка кадров |
Анализ практической работы предприятия. Выявление возможностей и способностей работающих в отношении квалификации и мастерства. Подготовка, профессиональное обучение кадров. Документирование обучения. |
Руководство предприятием. Руководители производств. |
Проверить выполнение и документацию. |
Из таблицы следует, что контроль производственного процесса представляет собой совокупность планируемых и систематически проводимых мероприятий, создающих необходимые условия для выполнения каждого этана процесса по обеспечению качества производимой продукции
Примером управления процессом может служить статистическое регулирование технологического процесса с помощью контрольных карт. Этот метод позволяет предупреждать появление дефектов или отклонений и является предпочтительным перед методами, связанными с уже случившимися отклонениями.
В соответствии с идеологией стандартов ИСО серии 9000 система качества должна функционировать таким образом, чтобы обеспечить уверенность в том, что проблемы предупреждаются, а не выявляются после возникновения.
В определении требований, предъявляемых к качеству продукции, ведущую роль играет функция маркетинга. Она должна:
- определять потребности в продукции;
- давать точное определение рыночного спроса и реализации, поскольку это важно для оценки нужного количества продукции, ее стоимости и сроков производства;
- давать четкое определение требований потребителя на основе постоянного анализа хозяйственных договоров, контрактов и потребностей рынка;
- четкое информирование обо всех требованиях, предъявляемых потребителем.
Функция маркетинга должна устанавливать на постоянной основе систему обратной связи и контроля получаемой информации. Вся информация, относящаяся к качеству продукции, должна анализироваться, сравниваться, интерпретироваться и доводиться до сведения в соответствии с установленными процедурами; подобная информация помогает определить характер и объем проблем, связанных с продукцией, на основании опыта и пожеланий потребителя. Кроме того, обратная связь с потребителем может явиться средством получения данных, необходимых как для внесения возможных изменений в производство, так и для соответствующих действий руководства.
Сырье, материалы, комплектующие детали и узлы, закупленные предприятием, становятся частью выпускаемой им продукции и оказывают непосредственное влияние на качество конечной продукции. Предприятие несет ответственность за качество конечной продукции в целом независимо от качества закупленных им материалов, полуфабрикатов и комплектующих изделий.
С целью обеспечения качества поставок система качества как минимум должна включать следующие элементы:
- четкое установление требований к покупным материалам, полуфабрикатам, комплектующим деталям и узлам;
- процедуры, методы и формы работы с поставщиками;
- входной контроль;
- процедуры согласования с поставщиками планов входного контроля;
- процедуры и положения решения спорных вопросов по качеству покупной продукции и ведения претензионной работы;
- регистрацию данных о качестве покупной продукции и оценку поставщиков.
В соответствии со стандартами ИСО серии 9000 все элементы, требования и положения, принятые предприятием для общего руководства и системы качества, должны быть документированы.
Такая документация обеспечивает единое понимание политики, задач в области качества и процедур по обеспечению, управлению и улучшению качества, позволяет четко разделить ответственность, права и обязанности по качеству, установить порядок взаимодействия подразделений и исполнителей при исполнении своих функций по качеству.
На предприятиях может быть комплект документов вида «руководство по качеству»:
общее руководство по качеству;
руководство по качеству различных производств (по видам продукции);
руководство по качеству различных подразделений;
руководство по качеству для различных этапов жизненного цикла и функций, например, при проектировании продукции, материально-техническом снабжении и др.
Основным назначением руководства по качеству является общее описание системы обеспечения качества, управления качеством и улучшения качества. Руководство по качеству выполняет функцию постоянного справочного материала при внедрении системы, поддержания его в рабочем состоянии и совершенствовании.
Система документации может быть построена на базе стандартов предприятия, отражающих выполнение различных функций и работ.
Подготовка производства должна давать уверенность в том, что технологический процесс и состояние элементов производства (оборудования, материалов и комплектующих, технологической оснастки и инструмента, производственного персонала, вспомогательных материалов, технической документации, производственной среды) обеспечат изготовление продукции в соответствии с требованиями технической документации.
Управление производственными процессами должно быть направлено на обеспечение качества продукции во время производства и, если это необходимо, при монтаже.
Производственные операции должны быть достаточно подробно определены в документированных рабочих инструкциях.
Общие принципы, используемые при эксплуатации производственного оборудования, должны быть зафиксированы и на них следует делать ссылки в индивидуальных рабочих инструкциях, отражающих критерии удовлетворительного выполнения конкретной работы и соответствия стандартам, регламентирующим качество выполнения работы. Стандарты качества работы должны быть достаточно подробно определены на основе письменно оформленных правил «фотографий» рабочего дня и (или) физических образцов.
Проверка качества продукции, процесса, программного обеспечения, материалов или производственной среды должна проводиться в чувствительных точках производства с целью минимизации последствий в итоге допущенных ошибок и максимизации эффективности.
Примером методики, облегчающей управление производством или процессом, может служить применение карт и планов контроля.
Проверка на каждом этапе должна быть связана с соответствующей документацией на продукцию или требованиями, установленными технологическим регламентом.
Если проверка характеристик технологического процесса не представляется технологически выгодной или возможной, производится проверка самой продукции. Во всех случаях должна устанавливаться взаимосвязь между контролем качества в процессе производства и документацией на процесс и конечную продукцию. Подобная организация работ должна быть доведена до сведения персонала, занимающегося производством и техническим контролем, и отражена в соответствующей документации.
Технологические процессы должны проверяться на способность производить продукцию в соответствии с установленными техническими условиями. Определяются операции, связанные с технологическими характеристиками и характеристиками продукции, существенно влияющими на качество.
Необходимо установить соответствующее управление, например, статистическое регулирование техпроцессов, чтобы их характеристики не выходили за рамки технических условий и технологического регламента.
Если это имеет значение для качества продукции, то вспомогательные материалы и средства, такие как вода, сжатый воздух, электроэнергия и химические продукты, используемые в производстве, должны подвергаться постоянным управляющим воздействиям и проверкам, чтобы обеспечить постоянство их воздействия на производство продукции. Когда производственная среда имеет важное значение для качества продукции, следует определить, управлять и проверять соответствующие пределы изменения условий (например, температуры, влажности, чистоты).
В процессе производства следует соответствующим образом хранить, разделять, транспортировать и защищать материалы для сохранения на должном уровне их функциональной пригодности. Особое внимание уделяется условиям хранения. Когда прослеживаемость материалов на производстве имеет важное значение для качества, идентификацию необходимо проводить в ходе всего производственного процесса в целях обеспечения прослеживаемости вплоть до исходной идентификации материала и статуса его качества.
Все производственное оборудование, включающее стационарные механизмы, зажимные приспособления, инструменты, крепления, модели и шаблоны, следует проверять на точность и соответствие номиналам до их ввода в эксплуатацию.
Особое внимание следует уделять ЭВМ, используемым для управления производственными процессами, и техническому обслуживанию программного обеспечения.
В промежутках между его эксплуатацией оборудование должно храниться и сохраняться в необходимых условиях, а также подвергаться повторной калибровке через необходимые интервалы времени для его соответствия номиналам и точности. Стабильность процесса обеспечивается разработкой программы профилактического технического обслуживания. Особое внимание следует уделять характеристикам оборудования, влияющим на основные характеристики качества продукции.
Определяется круг лиц, санкционирующих внесение изменений в технологический процесс; в случае необходимости эти изменения согласовываются с заказчиком. Все изменения в технологической оснастке и оборудовании, материалах и технологическом процессе должны найти отражение в документации.
Продукция должна оцениваться после каждого изменения с тем, чтобы проверить, что внесение изменения произвело рассчитанный эффект на качество продукции. Любое изменение соотношений между процессом и характеристиками продукции, являющееся результатом внесения таких изменений следует отражать в документах.
Контроль качества продукции не следует обязательно связывать с приемкой или контролем только готовой продукции. Он может применяться для оценки качества сырья, материалов, полуфабрикатов и комплектующих изделий, поступающих от поставщиков, при оценке качества закупок (в т.ч. входной контроль), при оценке качества изготовления продукции в процессе ее производства, при оценке качества готовой продукции, продукции, находящейся на хранении, после ее транспортирования в ремонте и после ремонта и т.д., т.е. в тех случаях, где надо решить вопрос, соответствует или не соответствует продукция установленным требованиям.
Основными задачами контроля являются обеспечение:
- достоверности оценки качества продукции, предъявляемой на контроль;
- однозначности взаимного признания результатов оценки качества продукции поставщиком и потребителем, инспекцией по качеству и другими контролирующими органами, осуществляющими контроль по одним и тем же планам и в одинаковых условиях.
Соответственно участок или цех-изготовитель продукции по отношению к участку, цеху, выполняющему последующие технологические операции, следует рассматривать как поставщика данной продукции.
Контроль качества продукции может быть сплошным, выборочным (статическим) и непрерывным (с чередованием сплошного и выборочного контроля).
При назначении сплошного контроля каждую единицу продукции в контролируемой партии, потоке следует подвергнуть контролю с целью выявления дефектных единиц продукции и принятия решения о пригодности продукции к поставке и (или) использованию по назначению.
При назначении выборочного статистического контроля из контролируемой партии продукции в соответствии с планом выборочного контроля следует извлечь случайным образом выборку (пробу), по результатам контроля, которой принимаются решения о пригодности к поставке и (или) использованию по назначению всей контролируемой партии продукции.
Правила отбора единиц продукции в выборку следует осуществлять по ГОСТ 18321-73.
При назначении непрерывного контроля каждую из единиц продукции следует подвергнуть контролю в той последовательности, в которой они производятся, до тех пор, пока не будет получено установленное планом контроля количество годных последовательно произведенных единиц продукции. После этого сплошной контроль прекращается и переходят на выборочный (статистический).
При непрерывном контроле продукция проступает на контроль в последовательности, в которой она производится, а не сформированными партиями.
По возможности дальнейшего использования проконтролированной продукции контроль может быть разрушающий и неразрушающий.
Разрушающий контроль может осуществляться только при выборочном (статистическом) контроле продукции.
Неразрушающий контроль может быть использован как при сплошном, так и выборочном (статистическом) контроле продукции.
По характеру предъявления продукции на контроль следует различать одиночные, последовательные партии и отдельные виды продукции.
При предъявлении единичных партий продукции решение о соответствии или несоответствии продукции установленным требованиям следует принимать по результатам контроля или испытаний только этой партии.
При предъявлении на контроль последовательно поступающих партий продукции решение о соответствии или несоответствии продукции установленным требованиям следует принимать по результатам контроля или испытаний данной партии с учетом предшествующих партий.
При предъявлении на контроль отдельных единиц продукции решение о соответствии или несоответствии продукции установленным требованиям следует принимать по каждой единице продукции отдельно.
По контролируемому признаку различают количественный, качественный и альтернативный.
Планы выборочного статистического контроля рекомендуется устанавливать в соответствии с требованиями государственных стандартов на статистический приемочный контроль и рекомендациями по статистическому регулированию технологических процессов.
Под входным контролем продукции следует понимать контроль продукции поставщика, поступивший к потребителю или заказчику и предназначенной для использования при изготовлении, ремонте или эксплуатации продукции.
Основными документами по организации и проведению входного контроля являются:
ГОСТ 24297-87 «Входной контроль продукции. Основные положения»;
Действующие НТД на данную продукцию, в том числе и на методы контроля и испытания ее;
Планы выборочного контроля по ГОСТ 18242-72, ГОСТ 20736-75, ГОСТ 16493-70;
Правила отбора единиц продукции в выборку по ГОСТ 18321-73. Обоснование и выбор планов выборочного контроля - по РД 50-605-86; Р 50-110-89.
Основными документами по оценке качества продукции в процессе ее производства являются:
действующие нормативно-технические и методические документы на данную продукцию, в том числе на методы контроля и испытания;
планы выборочного контроля по ГОСТ 18242-72, ГОСТ 20736-75, ГОСТ 24660-81, ГОСТ 16493-70, правила отбора единиц продукции в выборку - по ГОСТ 18321-73.
Основными документами по регулированию технологических процессов может служить:
действующая на предприятии технологическая документация.
Основными документами по хранению продукции в процессе контроля на предприятии могут служить:
1) действующие положения о производственных цехах и участках;
2) действующая на предприятии технологическая документация.
В соответствии с ГОСТ 16504-81 под окончательным контролем следует понимать контроль продукции, по результатам которого принимается решение о ее пригодности к поставкам и (или) использованию.
Требования к окончательному контролю и испытаниям устанавливаются:
в действующих на предприятии НТД на данный вид продукции;
в ГОСТ 18242-72, ГОСТ 20736-75, ГОСТ 16493-70, ГОСТ 24660-81;
Правилами отбора единицы продукции в выборку - по ГОСТ 18321-73;
Обоснованиями и выбором планов выборочного контроля - по РД 50-605-86;
Рекомендациями «построение и содержание разделов «Правила приемки» и «Методы контроля (анализа, испытаний, измерений)» в стандартах и технических условиях на продукцию»;
Р 50-110-89.
Порядок отправки продукции (в т.ч. на склад готовой продукции) после окончательного контроля и испытаний устанавливается самим предприятием.
Система регистрации результатов контроля и испытаний устанавливается самим предприятием на основе:
1) ГОСТ 24297-87;
2) Рекомендаций «Построение и содержание разделов «Правила приемки» и методов контроля (анализа, испытаний, измерений) в стандартах и технических условиях на продукцию».
Требования к используемым для контроля качества и испытаний продукции средствам измерений, методам выполнения измерении, порядку их аттестации и проверки и другим метрологическим правилам должны соответствовать стандартам и НТД Государственной системы единства измерений (ГСИ).
Единицы или партии продукции, подозреваемые в несоответствии, должны немедленно идентифицироваться и регистрироваться. Идентификация должна касаться также документации, по которой эту продукцию производят. Во всех случаях, когда это возможно, следует проводить обследование предыдущих партий продукции.
Несоответствующие единицы продукции должны быть отделены от продукции, отвечающей предъявленным требованиям, всякий раз, когда есть такая возможность, и адекватно идентифицированы для предупреждения их использования в дальнейшем до принятия соответствующих решений.
Идентификация и изоляция несоответствующей продукции должны проводиться в той точке технологического процесса, где обнаружено конкретное несоответствие, при этом необходимо выявить конкретное место и время появления несоответствия, чтобы можно было предупредить появление этих несоответствий в других единицах или партиях продукции и изъять их из дальнейшей переработки или использования.
Частным случаем несоответствующей продукции является дефектная продукция, а несоответствия - дефект.
Утилизацию несоответствующей продукции следует производить, как только это представится возможным, в соответствии с установленными требованиями. Решения по использованию единиц продукции и том виде, как они есть (без переработки), должны сопровождаться соответствующими документами с указанием обоснования этого решения и необходимых мер предосторожности.
Стадии обработки несоответствующих единиц продукции должны фиксироваться в виде документированных процедур с указанием форм маркировки, формуляров и отчетов.
Следует предпринимать соответствующие меры, предупреждающие возникновение повторного несоответствия. Необходимо рассмотреть вопрос о создании картотеки несоответствий, обеспечивающей анализ и выявление проблем общего характера в противовес случайным причинам. Примером такой картотеки является классификатор дефектов продукции, часто с указанием их первопричин.
Корректирующие воздействия организуются и проводятся при обнаружении каких-либо отклонений от установленных требований. Этими отклонениями могут быть дефекты продукции, обнаруженные на различных стадиях жизненного цикла продукции, неудовлетворительное состояние оборудования и оснастки, отсутствие на рабочем месте необходимой технической документации, недостаточный уровень квалификации персонала и т.д.
Меры корректирующего воздействия применяются как по отношению к объектам, в которых обнаружены отклонения (например, исправление дефектов продукции), так и по отношению к причинам, вызвавшим эти отклонения.
Следовательно, для проведения корректирующих воздействий необходим анализ причин. Возможна последовательная цепь причин, которые привели в конечном итоге к данному отклонению, поэтому система качества должна предусматривать организацию многоступенчатого анализа с тем, чтобы выявить все причины, вплоть до первопричины.
Следует определять важность дефектов продукции и их причин с точки зрения их потенциального влияния на издержки производства, затраты на обеспечение качества, эксплуатационные характеристики, надежность, безопасность и удовлетворение потребителя.
Корректирующие воздействия могут проводиться как по единичной информации о дефектах и иных отклонениях, так и по результатам выявления динамики на основе обработки накапливаемой информации. При этом широко могут быть использованы статистические методы и средства вычислительной техники.
В системе качества должны быть разработаны процедуры проведения анализа причин различных отклонений, оценки их последствий и принятия решений о корректирующих воздействиях.
Целесообразно, чтобы координация работ по данному комплексу вопросов была возложена на одно из подразделений предприятия (например, отдел контроля качества), в то время как участие в анализе, подготовке и выполнении могут принимать все подразделения предприятия.
При выработке корректирующих мер воздействия следует предусматривать меры, направленные на профилактику и предупреждение повторных появлений в будущем подобных отклонений.
Изменения, которые являются результатом мер корректирующего воздействия, следует фиксировать в рабочих инструкциях, документах на производственные процессы, технических условиях на продукцию и (или) систему качества.
Необходимо контролировать выполнение мер корректирующего воздействия и оценивать эффективность их воздействий.
Требования к проведению погрузочно-разгрузочных работ, упаковке, хранению и поставке продукции оговариваются в нормативно-технической документации на конкретный вид продукции.
Процедуры, обеспечивающие погрузочно-разгрузочные работы, хранение, упаковку и поставку продукции, должны быть направлены на создание условий для максимально-возможного сохранения и восстановления уровня качества продукции. Выполнение этих процедур должно быть тщательно спланировано.
Продукция должна иметь четкую маркировку и правильное этикетирование, исключающее неправильные погрузочно-разгрузочные работы, хранение, складирование и транспортирование, а также ее отправку.
Погрузочно-разгрузочные работы с материалами и готовой продукцией требуют правильного планирования и наличия нормативно-технической документации на эти работы, их контроля и периодического анализа.
Методы проведения погрузочно-разгрузочных работ должны предусматривать наличие соответствующих требований к поддонам, контейнерам, конвейерам, транспортным средствам, предупреждающих нанесение ущерба в связи с вибрацией, ударами, абразивным износом и коррозией, несоответствием температуры, влаги и другими отрицательными факторами, возникающими во время погрузочно-разгрузочных работ.
Содержание этих требований должно быть изложено в специально разработанной нормативно-технической документации и может быть оговорено в условиях договора между поставщиком и потребителем.
Предприятие-изготовитель должно иметь надежные склады и помещения для хранения продукции, исключающие нанесение ущерба или порчи до ее отправки или использования потребителем.
Поставщик должен разработать и использовать процедуры проверки складирования продукции, которые должны предупреждать и выявлять возможную ее порчу.
Все стандарты по обеспечению качества содержат требование контролировать регистрируемые данные:
- отчеты по результатам аудита;
- результаты контроля, производимого в соответствии с планом контроля и испытаний;
- данные о надежности источника поставок;
- сертификаты на материалы;
- данные о проверке контрольно-измерительного и испытательного оборудования;
- документацию на изделия, не соответствующие ТУ;
- информацию о корректирующих действиях;
- результаты контроля складских запасов;
- результаты испытаний и проверок, проводимых заказчиками и регулирующими органами или иной третьей стороной;
- данные об аттестации персонала;
- протоколы функциональных испытаний;
- протоколы установочных и предпусковых испытаний и др.
Все отчеты, протоколы и другие записи должны храниться в течение срока, установленного законодательством или контрактными документами, в условиях, обеспечивающих их надежную защиту от повреждения и утери. Обычно это помещения со стальными дверями, защищенные от воды и возгорания. По согласованию с заказчиком могут быть и другие способы хранения: компьютеризированное хранение, хранение микрофильмов и микрофиш.
Приложение 12
Идентификация и прослеживаемость продукции на предприятии
Один их важнейших элементов системы качества является механизм идентификации, позволяющий обеспечить прослеживаемость продукции по всему технологическому циклу изготовления продукции.
Идентификация, в соответствии с идеологией стандартов ИСО 9000, распространяется на материалы, сырье, комплектующие изделия, готовую продукцию, контрольно-измерительные приборы, документацию и т.д.
Идентификация - процедура, предполагающая маркировку и этикетирование сырья, материалов, комплектующих изделий, готовой продукции (единицы, партии и т.д.), а также технической и технологической документации на них, обеспечивающих прослеживаемость использования и местонахождение объекта с целью выявления возможных причин брака изготовленной продукции или дефектов производственных и технологических процессов.
Процедура прослеживаемости и идентификации должны обеспечить возможность:
определения места и времени появления дефекта;
определение местонахождения всего объема продукции с выявленным дефектом;
отзыва, изоляции и учета дефектной продукции;
проведения оперативного и систематического анализа причин дефектов и выработки корректирующих воздействий;
учета продукции для целей оперативного управления производства.
Обеспечение прослеживаемости достигается за счет маркирования объекта идентификации, внедрения сопроводительных документов (маршрутные карты, сопроводительные талоны и т.д.) и других носителей информации, а также последовательной регистрации данных об объекте идентификации по всей технологической цепочке от поступления на предприятие материала и комплектующих изделий до упаковки и отправки готовой продукции.
Регистрация данных об объектах идентификации осуществляется персоналом при запуске материала или заготовок в производство, передаче деталей на склад или смежный цех для последующей обработки, проведении контроля качества изготовленных деталей для сборочных единиц, учета и изоляции несоответствующей продукции, упаковке готовой продукции и т.д.
Особое значение идентификация готовой продукции имеет для подтверждения статуса контроля и испытаний.
«Факт проверки материалов и узлов должен идентифицироваться в течение всего производственного процесса. Такая идентификация может осуществляться с помощью штампов, этикеток, ярлыков, надписей, системы обозначений, транспортных упаковочных единиц или же сопроводительных контрольных карт. Такая идентификация позволяет отличить проверенный материал от непроверенного и установить факт приемки продукции на данном этапе проверки. Кроме того, она также обеспечивает прослеживаемость до следующего звена, ответственного за операцию» (ИСО 9004).
«Единицы продукции или партии продукции, подозреваемые в несоответствии, должны немедленно идентифицироваться и регистрироваться»... (ИСО 9004).
В процессе производства осуществляется движение двух потоков: материального (сырья, материалов, деталей, узлов и т.д.) и информационного (данных о сырье, материалах, деталях, узлов и т.д. на бумажных и других носителях, сопровождающих материальный поток).
Необходимым условием достижения эффективного механизма прослеживаемости по всему производственному циклу, начиная с поступления материалов и комплектующих изделий от поставщиков и кончая отгрузкой готовой продукции, является обеспечение однозначной связи материального и информационного потоков в процессе производства продукции.
В зависимости от условий производства идентификация может быть либо индивидуальной, либо партии (групповой).
Индивидуальная идентификация предполагает маркировку и прослеживание непосредственно каждой детали или сборочной единицы с помощью, например, бирок, ярлыков или клеймения.
Групповая идентификация предполагает маркировку совокупности комплектующих изделий, заготовок, деталей или материала либо в размере партии, либо ее части, либо комплекта в сборочном производстве. В этом случае соответствующей маркировке подвергается технологическая тара (связка металла бухта и т.д.) в которой по технологической цепочке движется строго определенное количество заготовок или деталей. Эта идентификация характерна для массового производства.
Сквозной характер механизма идентификации и прослеживаемости по всему производственному циклу обеспечивается увязкой:
- способов маркировки и содержания сопроводительной документации на материалы и комплектующие изделия с внутризаводской маркировкой и содержанием сопроводительных документов (носителей информации) на детали, сборочные единицы, готовые изделия;
- способов внутризаводской индивидуальной и (или) групповой идентификации деталей, сборочных единиц, готовых изделий;
- способов внутризаводской маркировки и содержания сопроводительных документов (носителей информации) с маркировкой упакованной и отгруженной продукции и содержанием сопроводительной и эксплуатационной документации.
В соответствии с принципами системы качества процедуры идентификации и прослеживаемости на предприятии должны быть объектом внутренней проверки.
При организации и проведении работ по идентификации и прослеживаемости следует руководствоваться технической и экономической целесообразностью внедрения того или иного способа идентификации с учетом анализа производственных затрат на качество.
Комплекс работ по разработке и внедрению на предприятии процедур идентификации и прослеживаемости включает следующие взаимосвязанные направления:
- техническое (технологическое) обеспечение;
- информационное обеспечение;
- организационное обеспечение.
Процедуры идентификации и прослеживаемости продукции должны быть документированы.
Комплекс работ по техническому (технологическому) обеспечению идентификации и прослеживаемости на предприятии включает разработку технологии маркирования применительно к конкретным объектам идентификации.
Маркирование представляет собой процесс нанесения на объект идентификации соответствующей информации в виде совокупности знаков, шрифтов, символов и т.д., отражающих отличительные признаки материала, детали или изделия и позволяющих обеспечить прослеживаемость.
Маркировка как результат маркирования подразделяется на словесную (слово, буква, цифра, символ), изобразительную (рисунок, фигура и т.д.), пространственную (рельефное изображение) и комбинированную. Одной из разновидностей маркирования является прикрепление к материалу или детали специально изготовленных табличек, бирок, шильдиков, на которые наносится информация, характеризующая материал или деталь.
Способы маркирования должны быть частью технологического процесса изготовления продукции и регламентироваться в соответствующей технической документации.
Способы маркирования объектов идентификации (механические, физико-химические, электрофизические и т.д.) не должны ухудшать показатели качества материала, детали, сборочной единицы, готового изделия.
Как элементы технологического процесса изготовления продукции способы маркирования должны быть объектом операционного контроля с применением различных форм периодического, летучего, инспекционного контроля.
Технические средства, применяемые для выбранного способа маркировки (штампы, клейма и т.д.) должны поддерживаться в работоспособном состоянии и храниться в условиях, исключающих возможность их бесконтрольного использования персоналом. Необходимо четко определить круг должностных лиц, имеющих доступ к указанным средствам и осуществляющим контроль за их использованием.
При разработке технологии применения отдельных способов маркировки, например, электрохимического, радиоактивного, ультразвукового, адгезионного и некоторых других, необходимо обеспечить соответствие применяемых методов требованиям производственной гигиены и безопасности.
Маркировка в виде совокупности знаков, символов, характеризующих изделие посредством бирок, ярлыков, клейм и т.д. должна быть доступной для использования персоналом, легко читаемой и не допускать неоднозначного понимания; исключать возможность фальсификации (подделки) и сохраняться в процессе производства, изоляции, хранения и упаковки продукции.
Персонал, связанный с работами по идентификации и прослеживаемости должен пройти подготовку и обучение по технологии применения выбранных способов маркировки, знать расшифровку применяемых в процессе идентификации шифров, кодов и обозначений.
Информационное обеспечение идентификации и прослеживаемости включает в себя разработку и внедрение информационных форм (сопроводительных документов и других носителей), схем, информационных потоков и точек регистрации информации, а также процедур обработки, систематизации, хранения и реализации данных об объектах идентификации, включая компьютерные способы обработки информации.
Вид, состав и содержание носителей информации для идентификации и прослеживаемости в каждом отдельном случае определяется выбранным методом идентификации и способом маркировки материала, деталей, изделий в процессе производства и спецификой конкретной продукции.
Сопроводительная документация, используемая в целях идентификации и прослеживаемости должна быть адресной и удовлетворять принципу информационной достаточности, обеспечивать преемственность процессов идентификации; должна быть доступной и сохраняемой по всей технологической цепочке, иметь определенный уровень утверждения на предприятии.
Адресность заключается в четком и однозначном регламентировании в документах источников и потребителей сопроводительных документов (информации) - склад, цех, участок, исполнитель.
Информационная достаточность заключается в наиболее полном отражении в сопроводительных информационных формах таких характерных признаков (характеристик) объекта идентификации (материал, деталь, изделие), которые позволили бы однозначно осуществить идентификацию объекта на конкретном технологическом маршруте, а при перенесении данных в последующие информационные формы обеспечить прослеживаемость по всей технологической цепочке.
Преемственность последующих и предыдущих сопроводительных документов в процессе идентификации означает, что основные данные из предыдущих форм должны быть перенесены в последующие для сохранения отличительных характерных признаков объектов идентификации при осуществлении прослеживаемости.
Доступность сопроводительных документов заключается в обеспечении свободного доступа ответственных лиц и персонала к сопроводительным документам, свободного владения способами заполнения, оформления, учета, хранения этих документов в процессе производства.
Сохраняемость сопроводительных документов заключается в обеспечении условий сохранности их в процессе производства по всей технологической цепочке и организации хранения документов на определенный период времени в специально отведенном месте (на складе, в цехе и т.д.)
Для идентификации и прослеживаемости на предприятиях могут быть применены следующие документы:
- сопроводительный талон, предназначенный для выдачи всех материалов с центрального склада в цеховые склады;
- маршрутный лист, предназначенный для указания состава и последовательности операций по маршруту изготовления деталей;
- сопроводительный талон, предназначенный для сдачи всех готовых деталей на склад готовых деталей;
- сопроводительный лист, предназначенный для указания состава и последовательности выполняемых операций по маршруту;
- технологический паспорт, предназначенный для указания последовательности и содержания операций, выполняемых при изготовлении изделия, включая операционный и приемочный контроль.
Сопроводительный талон 1 предназначен для выдачи всех материалов с центрального склада и получения их в материальные склады цехов.
Сопроводительный талон 1 содержит следующие реквизиты:
- марка;
- партия;
- количество;
- номер контрольной карты;
- характеристика материала (с указанием срока годности);
- фамилия ответственного лица (кладовщика);
- дата поступления;
- срок и место хранения.
На сопроводительном талоне 1 должна быть предусмотрена виза контролера, подтверждающая качество материалов.
Маршрутный лист составляется на все детали, изготавливаемые в цехах. Из сопроводительного талона 1 в маршрутный лист вносятся следующие основные данные:
- наименование материала;
- марка;
- номер партии;
- наименование детали;
- обозначение детали;
- наименование изделия;
- название операций;
- Ф. И. О. рабочего;
- отметка ОТК о приемке деталей;
- отметка ОТК о приемке партий деталей.
Сопроводительный талон 2 содержит следующие реквизиты:
- Ф. И. О. исполнителя;
- тип изделия;
- наименование детали;
- номер детали;
- количество деталей;
- наименование материала;
- марка материала;
- номер партии;
- номер маршрутного листа;
- количество годных деталей;
- количество бракованных деталей;
- Ф. И. О. работника ОТК.
Основные данные сопроводительного талона 2 выписываются из предыдущего маршрутного листа.
Сопроводительный лист составляется на все детали и сборочные единицы. В нем указывается статус контроля и данные о качестве выполненных операций. Сопроводительный лист заполняется на основании сопроводительного талона 2 и содержит следующие основные реквизиты:
- наименование материала;
- наименование, обозначение, номер детали;
- наименование, обозначение, номер сборочной единицы;
- название операций;
- Ф. И. О. исполнителей;
- количество деталей, предъявленных ОТК;
- количество деталей, принятых ОТК;
- отметка (штамп) ОТК.
Технологический паспорт предназначен для указания последовательности и содержания операций, выполняемых при изготовлении изделия, включая операционный и приемочный контроль. Технологический паспорт является сопроводительным документом по всему указанному в нем технологическому маршруту изготовления изделия. В общем виде форма технологического паспорта содержит:
- наименование, обозначение, номер сборочной единицы;
- наименование, шифр изделия;
- номер сопроводительного листа;
- название операций сборки;
- Ф. И. О. исполнителей,
- отметка (штамп) ОТК.
Разработка схем информационных потоков и точек регистрации информации об объектах идентификации осуществляется на основе технологических маршрутов изготовления продукции, действующих схем и точек технического контроля с учетом специфики и трудоемкости операции контроля и способов обработки информации.
Процедуры обработки систематизации, хранения и реализации информации об объектах идентификации должны быть согласованы с действующими на предприятии процедурами по регистрации данных.
Организационное обеспечение идентификации и прослеживаемости на предприятии включает установление функциональных задач и ответственности подразделения и должностных лиц предприятия, разработку и документирование процедур идентификации и прослеживаемости обучение персонала и проведение внутренних проверок эффективности действующих процедур.
Планирование и организация работ на предприятии по идентификации и прослеживаемости осуществляется последовательно в комплексе работ по обеспечению качества продукции и охватывает все стадии процесса производства.
На этапе маркетинга в системе качества службы маркетинга решаются следующие основные задачи:
- подготовка предложений по идентификации новой продукции, исходя из требований рынка, в кратком описании продукции (ТЗ, техническое предложение);
- подготовка предложений по применению идентификации для выявления, отзыва и изоляции дефектной продукции на стадиях реализации и эксплуатации.
На этапе проектирования и разработки продукции конструкторскими и технологическими службами осуществляется:
- разработка требований по применению индивидуальной или партионной (групповой) идентификации материалов, комплектующих изделий, деталей, сборочных единиц, готовой продукции, исходя из специфики и характера продукции и производства;
- разработка требований к способам маркирования и составу сопроводительных документов;
- подготовка предложений по номенклатуре наиболее ответственных деталей, сборочных единиц, подлежащих индивидуальной идентификации;
- проведение технико-экономического обоснования применения методов идентификации.
На этапе материально-технического снабжения службой осуществляется:
- определение оптимальных размеров партий материалов и комплектующих изделий и графиков их поставок по срокам и объемам в целях идентификации и прослеживаемости при запуске в производство;
- согласование с поставщиками методов идентификации, способов маркировки материалов и комплектующих изделий, а также состава и содержания сопроводительной документации;
- установление порядка складирования, хранения и выдачи в производство материалов и комплектующих, в т.ч. для изделий, имеющих ограниченный срок хранения и использования,
- разработка и систематический контроль совместно с ОК выполнения процедур идентификации поступающего материала и комплектующих по всей технологической цепочке, а также процедур идентификации несоответствующей продукции (при входном контроле), ее хранения и изоляции;
- разработка форм сопроводительных документов и других носителей информации и соответствии с принятыми методами и способами идентификации и прослеживаемости на предприятии;
- обеспечение совместно с другими подразделениями увязки и преемственности между маркировкой материалов и комплектующих изделий и записями в сопроводительной документации с технологической маркировкой и записями во внутренних носителях информации;
- организация учета, систематизации, хранения и использования данных по идентификации материалов, комплектующих изделий и сопроводительных документов.
На этане подготовки к разработке производственных процессов технологическими службами совместно с производственными подразделениями осуществляются:
- разработка схем идентификации;
- отработка и проверка в опытном производстве практических методов и способов идентификации материалов и комплектующих при запуске в производство деталей, узлов, а также готовой продукции в процессе производства;
- разработка оптимальных межцеховых маршрутов и технологической тары с учетом требований идентификации;
- разработка и согласование с заинтересованными службами предприятия (ОМТС, ОК, ОГТ, ПТО и т.д.) технологических процессов идентификации и прослеживаемости документов, требований по учету, систематизации и обработке данных по идентификации;
- регламентирование отработанной технологии идентификации и прослеживаемости в нормативно-технической и методической документации;
- обучение персонала способам и методам идентификации, осуществляемое службой подготовки кадров;
- подготовка предложений по срокам хранения информации о материалах, комплектующих, готовой продукции в процессе идентификации.
На этапе производства производственными подразделениями осуществляется:
- обеспечение стабильного функционирования принятой схемы идентификации и прослеживаемости и контроль за соблюдением установленных процедур;
- корректировка принятых способов идентификации и состава сопроводительной документации по результатам данных о качестве продукции, анализа причин дефектов и отказов, анализа затрат на качество, предложений подразделений и служб предприятия и т.д.;
- обеспечение преемственности принятой схемы идентификации и прослеживаемости при внесении изменений в действующую техническую документацию;
- внедрение автоматизированных средств обработки данных по идентификации в процессе производства.
На этапе контроля и проведения испытаний службой ОК совместно с производственными подразделениями осуществляется:
- идентификация прошедшей контроль продукции по всей технологической цепочке;
- идентификация несоответствующей продукции (деталей, узлов, сборочных единиц и т.д.) с последующей изоляцией;
- контроль оформления и четкой записи информации в сопроводительной документации по процедурам контроля и испытаний.
На стадиях погрузочно-разгрузочных работ, упаковки, хранения и поставки осуществляется:
- маркировка, этикетирование отгружаемой продукции;
- идентификация изделий с ограниченным сроком годности;
- обеспечение четкого порядка складирования и отгрузки изделий с ограниченным сроком годности или требующих специальной защиты в процессе транспортировки и хранения;
- обеспечение однозначной связи между технологической маркировкой и записями во внутренних носителях информации с маркировкой упакованной и отгружаемой продукцией и записями в сопроводительной и эксплуатационной документации.
Работы по идентификации и прослеживаемости осуществляются на всех этапах петли качества и охватывают все основные элементы производства.
Обеспечение прослеживаемости достигается за счет маркирования объекта идентификации, внедрения сопроводительных документов (маршрутные карты, сопроводительные талоны и т.д.) или других носителей информации, а также последовательной регистрации данных об объекте идентификации по всей технологической цепочке от поступления на предприятие материала и комплектующих изделий до упаковки и отправки готовой продукции.
Комплекс работ по разработке и внедрению на предприятии процедур идентификации и прослеживаемости включает следующие взаимосвязанные направления:
- техническое (технологическое) обеспечение;
- информационное обеспечение;
- организационное обеспечение.
Состав задач технологического обеспечения приведен на рис. 1.
Рис. 1.
Состав работ по информационному обеспечению приведен на рис. 2.
Рис. 2.
Состав основных работ по организационному обеспечению приведен на рис. 3.
Рис. 3.
Требования GMP по маркировке.
Таблица № 3
|
|
Стерильный |
Не стерильный |
|
Индивидуальная упаковка |
|
|
|
Наименование изделия |
х |
х |
|
Пометка «СТЕРИЛЬНО» |
х |
- |
|
Пометка «ОДНОКРАТНОГО ПРИМЕНЕНИЯ» |
х |
х |
|
Наименование производителя/поставщика и его адрес |
х |
х |
|
Номер партии |
х |
х |
|
Инструкция по применению (если требуется) |
х |
х |
|
Меры предосторожности при использовании (если есть) |
х |
х |
|
Срок годности |
х |
х |
|
Контейнер групповой упаковки |
|
|
|
Наименование изделия |
х |
х |
|
Пометка «СТЕРИЛЬНО» |
х |
- |
|
Наименование и адрес производителя /поставщика |
х |
х |
|
Номер партии |
х* |
х |
|
Дата стерилизации (год, мес.) |
х* |
- |
|
Срок годности |
х |
х |
|
Инструкция по хранению (если есть) |
х |
х |
* если номер партии точно отражает дату стерилизации (год, месяц), то она не обязательно должна быть проставлена на упаковке и наоборот.